
分析 (1)根据质量守恒定律解答;根据在化合物中正负化合价代数和为零,结合高铁酸钾的化学式进行解答即可;
(2)根据将硬水软化成软水的方法是加热煮沸解答;
(3)根据纯水在常压下的沸点为1000C,可通过测定沸点的方法证明是否为纯水,强酸强碱盐的水溶液pH=7,电解活泼金属的含氧酸盐时,得到H2、O2,体积比为2:1,以此解答该题.
(4)①根据生石灰与水反应生成氢氧化钙解答;根据甲、乙、丙的溶解度随温度的变化情况分析;
②根据在饱和溶液中溶液的浓度与溶解度的关系分析;
③根据甲、乙、丙的溶解度随温度的变化情况及溶解度与溶质的质量分数关系分析.
解答 解:(1)由2Fe(OH)3+3Cl2+10KOH═2K2FeO4+6X+8H2O,根据质量守恒定律,化学反应前后原子的种类和数目不变,反应前Fe、O、H、Cl、K的原子个数分别是2、16、16、6、10;反应前Fe、O、H、Cl、K的原子个数分别是2、16、16、0、0,则6X中有6个K和6个Cl,则X的化学式为KCl;
因为钾元素显+1价,氧元素显-2价,则设铁元素的化合价是x,根据在化合物中正负化合价代数和为零,可得:(+1)×2+x+(-2)×4=0,则x=+6价.
(2)自来水厂净化水的过程不能将硬水软化成软水.
(3)
A、纯水在常压下的沸点为1000C,可通过测定沸点的方法证明是否为纯水,故正确;
B、强酸强碱盐的水溶液pH=7,不能确定是否为纯水,故错误;
C.电解活泼金属的含氧酸盐时,得到H2、O2,体积比为2:1,不能确定是否含有纯水,故错误;
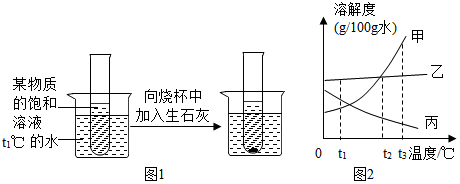
(4)①生石灰与水反应生成氢氧化钙,反应的化学方程式为CaO+H2O═Ca(OH)2;石灰与水反应放热,溶液温度升高,有晶体析出,说明物质的溶解度随温度的升高而降低,故选丙;
②由于在t2℃时,甲、乙的溶解度相同,则如果要配制相同浓度的甲、乙饱和溶液,需要把温度控制在t2℃.
③由甲、乙、丙三种固体物质的溶解度曲线可知,甲、乙的溶解度随温度的升高而增大,丙的溶解度随温度的升高而减小,所以将t3℃甲、乙、丙的饱和溶液分别降温到t1℃,甲、乙析出晶体,溶质的质量分数减小,丙变为不饱和溶液,溶质质量分数与降温前相等,据饱和溶液中质量分数的计算式$\frac{溶解度}{100g+溶解度}$×100%可知,t1℃时乙的溶解度大于甲的溶解度、大于t3℃时丙的溶解度,t1℃时甲的溶解度大于t3℃时丙的溶解度,所以此时所得溶液中溶质的质量分数由小到大的顺序是:丙<甲<乙.
答案:
(1)KCl;+6;
(2)不能;
(3)A;
(4)①CaO+H2O═Ca(OH)2;丙;②t2;③丙<甲<乙.
点评 本题比较细致地考查了净化水的方法及所用物质的用途,这就要求同学们在平时学习中要将问题学透彻,才能灵活运用.本题主要考查了学生对溶解度曲线意义的认识和掌握,同时须明确饱和溶液中溶质的质量分数的计算方法,要据相关知识细心解答.


科目:初中化学 来源: 题型:填空题
| 物质 | A | B | C | D |
| 反应前的质量/g | 6.4 | 3.2 | 4.0 | 2.8 |
| 反应后的质量/g | 5.2 | 待测 | 7.2 | 2.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | P+O2$\frac{\underline{\;点燃\;}}{\;}$PO2 | B. | Zn+MgCl2═ZnCl2+Mg | ||
| C. | 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑ | D. | HCl+Fe2O3═H2O+FeCl3 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 人类社会的可持续发展离不开能源和新型材料.
人类社会的可持续发展离不开能源和新型材料.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com