
| 实验步骤 | 实验现象 | 实验结论 |
| (3)取反应后烧杯中的溶液于试管,加入酚酞试液 | 猜想二不正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| (4) | 猜想四正确 |
分析 【提出猜想】
氢氧化钠和稀硫酸反应生成硫酸钠和水;
【实验探究】
氢氧化钠溶液显碱性,能使酚酞试液变红色;
稀硫酸显酸性,能使石蕊试液变红色;
【反思与交流】
烧杯中的溶液末经处理直接倒入下水道,可能会污染环境,腐蚀下水道等;
在分析化学反应后所得物质成分时,除考虑生成物外,还需考虑反应物是否过量.
解答 解:(1)稀硫酸和氢氧化钠恰好完全反应时,溶液中的溶质是硫酸钠;
如果稀硫酸过量,溶液中的溶质是硫酸和硫酸钠;
如果氢氧化钠过量,溶液中的溶质是氢氧化钠和硫酸钠.
故填:Na2SO4、H2SO4.
(2)通过分析,猜想三不合理,理由是氢氧化钠和硫酸不能共存.
故填:三;氢氧化钠和硫酸不能共存.
(3)取反应后烧杯中的溶液于试管,加入酚酞试液,酚酞试液不变色,说明猜想二不正确,实验过程如下表所示:
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后烧杯中的溶液于试管,加入酚酞试液 | 酚酞试液不变色 | 猜想二不正确 |
| 实验步骤 | 实验现象 | 实验结论 |
| 取反应后烧杯中的溶液于试管,滴加石蕊试液 | 石蕊试液变红色 | 猜想四正确 |
点评 合理设计实验,科学地进行实验、分析实验,是得出正确实验结论的前提,因此要学会设计实验、进行实验、分析实验,为学好化学知识奠定基础.


科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 结论 |
| 用试管取该溶液1-2mL,滴入1-2滴无色酚酞试液,振荡 | 无色酚酞试液变 | 溶液呈碱性 |
| 无色酚酞试液不变色 | 溶液呈 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
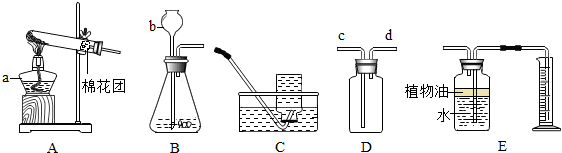
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
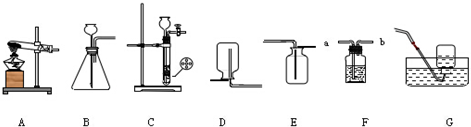
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
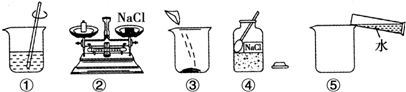
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 (1)如图所示,将二氧化碳倒入烧杯中.现象:烧杯中的蜡烛下面的先熄灭,上面的后熄灭;
(1)如图所示,将二氧化碳倒入烧杯中.现象:烧杯中的蜡烛下面的先熄灭,上面的后熄灭;查看答案和解析>>
科目:初中化学 来源: 题型:解答题
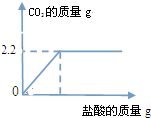 某校兴趣小组为探究石灰石中碳酸钙的质量分数,进行了下列实验:称取6.5g石灰石样品,再加入足量的稀盐酸,充分反应后(杂质不溶于水,也不与稀盐酸反应),产生的CO2和消耗的稀盐酸的质量关系如图所示.求:石灰石中碳酸钙的质量分数.
某校兴趣小组为探究石灰石中碳酸钙的质量分数,进行了下列实验:称取6.5g石灰石样品,再加入足量的稀盐酸,充分反应后(杂质不溶于水,也不与稀盐酸反应),产生的CO2和消耗的稀盐酸的质量关系如图所示.求:石灰石中碳酸钙的质量分数.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com