
分析 根据物质的俗称、分子结构、根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答;根据化合物中元素质量分数的计算方法来分析.
解答 解:乙醇俗称酒精;由乙醇的化学式可知,每个乙醇分子中含有2个碳原子、6个氢原子和1个氧原子;乙醇中碳、氢、氧元素的质量比为(12×2):(1×6):(16×1)=12:3:8;含3.6g碳元素需要乙醇的质量为:3.6g÷$\frac{12×2}{12×2+1×6+16}×100%$=6.9g.
故填:酒精2:6:1;12:3:8;6.9.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
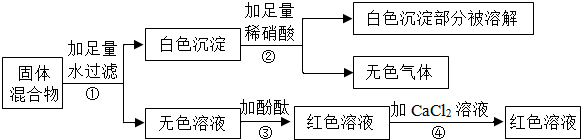
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
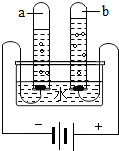 化学是人类用以认识和改造物质世界的主要方法和手段之一.
化学是人类用以认识和改造物质世界的主要方法和手段之一.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 物质 | A | B | C | D |
| 反应前质量/g | 20 | 20 | 20 | 20 |
| 反应后质量/g | 20 | 30 | X | 14 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 如图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题.
如图是甲、乙两种固体物质的溶解度曲线,试回答下列相关问题.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 | |
| 实验一 | 取过氧化氢溶液 ,然后将带火星的木条伸入装有过氧化氢溶液的试管中 | 木条不复燃 | 常温下过氧化氢溶液不分解 |
| 实验二 | 在装有过氧化氢溶液的试管中加入少量Al2O3,然后将带火星的木条伸入试管中 | 木条复燃 | Al2O3 能加快过氧化氢的分解速率 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 金属铝中,铝元素的化合价为﹢3价 | |
| B. | 化合物中非金属元素的化合价均显负价 | |
| C. | 有些元素在不同的条件下可表现出不同的化合价 | |
| D. | 化合价与原子的最外层电子数无关 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com