
| A. | 红色 | B. | 蓝色 | C. | 紫色 | D. | 无法确认 |
 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:推断题
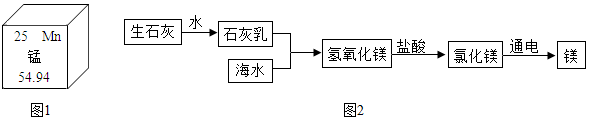
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | N2 | B. | CO2 | C. | CO | D. | SO2 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图,在盛有一定质量分数稀硫酸的容器中,放一塑料方块.刚好能悬浮于稀硫酸中,若向容器中加入少量氯化钡溶液后,则塑料方块在溶液中( )
如图,在盛有一定质量分数稀硫酸的容器中,放一塑料方块.刚好能悬浮于稀硫酸中,若向容器中加入少量氯化钡溶液后,则塑料方块在溶液中( )| A. | 下沉 | B. | 上浮 | C. | 不变 | D. | 无法判断 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 利用如图装置进行实验.
利用如图装置进行实验.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com