
 ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ
ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ| 100 |
| 44 |
| X |
| 4.4æĖ |
| 73 |
| 44 |
| Y |
| 4.4æĖ |
| 10æĖ |
| 12æĖ |
| 14.6æĖ |
| 73æĖ |



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
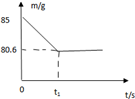 ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠĢ¼ĖįøʵÄŗ¬Į森ĻÖČ”12æĖ±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73æĖĻ”ŃĪĖį£¬³ä·Ö·“Ó¦£®£Ø±“æĒÖŠ³żĢ¼ĖįøĘĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£®²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Ø m £©Óė·“Ó¦Ź±¼ä£Ø t £©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬
ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠĢ¼ĖįøʵÄŗ¬Į森ĻÖČ”12æĖ±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73æĖĻ”ŃĪĖį£¬³ä·Ö·“Ó¦£®£Ø±“æĒÖŠ³żĢ¼ĖįøĘĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£®²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Ø m £©Óė·“Ó¦Ź±¼ä£Ø t £©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2010ÄźŗŚĮś½Ź”Ėē»ÆŹŠÖŠæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
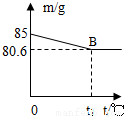 ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ
ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2010ÄźŗŚĮś½Ź”ĘėĘė¹ž¶ūŹŠÖŠæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
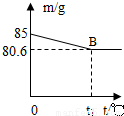 ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ
ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗ³õÖŠ»Æѧ Ą“Ō“£ŗ2010ÄźŗŚĮś½Ź”ĘßĢØŗÓŹŠÖŠæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗ½ā“šĢā
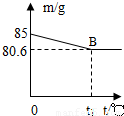 ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ
ijŠĖȤŠ”×é²ā¶Ø±“æĒÖŠCaCO3µÄŗ¬Į森ĻÖČ”l2g±“æĒµ·Ė飬·ÅČėÉÕ±ÖŠ£¬Č»ŗóĻņĘäÖŠ¼ÓČė73gÄ³ÖŹĮæ·ÖŹżµÄĻ”ŃĪĖį£¬Ź¹Ö®³ä·Ö·“Ó¦£Ø±“æĒÖŠ³żCaCO3ĶāµÄĘäĖū³É·Ö¶¼²»ČÜÓŚĖ®£¬ĒŅ²»ÓėĻ”ŃĪĖį·“Ó¦£©£¬²āµĆÉÕ±ÖŠµÄ·“Ó¦Ź£ÓąĪļµÄÖŹĮæ£Øm£©Óė·“Ó¦Ź±¼ä£Øt£©µÄ¹ŲĻµČēĶ¼ĖłŹ¾£ØŗöĀŌĖ®ÕōĘųµÄ»Ó·¢£©£¬ĘäÖŠµ±·“Ó¦½ųŠŠµ½BµćŹ±£¬ĖłÓĆĻ”ŃĪĖįøÕŗĆĻūŗÄĮĖ¼ÓČėĮæµÄŅ»°ė£®ŹŌ¼ĘĖć£ŗ²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com