
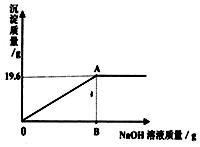
 有一包固体粉末,可能是 CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种.某实验小组同学先用托盘天 平称取 46.2 克该粉末,溶于水配成 174.6 克蓝色澄清 溶液,再往其中加入溶质质量分数为 8%的 NaOH溶液,产生沉淀的质量与所加 NaOH 溶液质量的关系如图所示.计算正好完全反应时所得溶液中溶质的质量分数.
有一包固体粉末,可能是 CaCO3、Na2SO4、CuSO4、Na2CO3中的一种或多种.某实验小组同学先用托盘天 平称取 46.2 克该粉末,溶于水配成 174.6 克蓝色澄清 溶液,再往其中加入溶质质量分数为 8%的 NaOH溶液,产生沉淀的质量与所加 NaOH 溶液质量的关系如图所示.计算正好完全反应时所得溶液中溶质的质量分数. 分析 根据加水溶解后得到的是蓝色溶液,可以知道在固体粉末中不含碳酸钙和碳酸钠,碳酸钠和硫酸铜不能共存进行分析;根据分析可以知道,该混合物可能是硫酸铜和硫酸钠的混合物,根据图象中所给数据,结合化学方程式为进行解答,注意质量守恒定律的应用.
解答 解:通过分析可以知道,该混合物可能是硫酸铜和硫酸钠的混合物,根据图象可知硫酸铜和氢氧化钠反应生成了沉淀的质量为9.8g
可以根据硫酸钡沉淀的质量来求出硫酸铜、氢氧化钠、生成的硫酸钠的质量,然后再根据硫酸铜的质量来判断是不是含有硫酸钠,进而求出反应后生成的硫酸钠溶液的质量分数,所以
设生成最大沉淀量时所加NaOH的质量为x,46.2 g粉末中含有CuSO4的质量为y,生成Na2SO4的质量为z
CuSO4+2NaOH=Na2SO4+Cu(OH)2↓
160 80 142 98
y x z 19.6g
$\frac{160}{y}=\frac{80}{x}=\frac{142}{z}=\frac{98}{19.6g}$
x=16g,y=32g,z=28.4g
所以NaOH溶液的质量═$\frac{16g}{8%}$=200g;
Na2SO4的质量=46.2g-32.0g=14.2g
正好完全反应时所得溶液中溶质的质量分数是=$\frac{28.4g+14.2g}{200g+174.6g-19.6g}$×100%=13%
答:正好完全反应时所得溶液中溶质的质量分数是13%.
点评 熟练掌握常见的盐的化学性质,记住它们的化学特性以根据实验现象作出正确的判断,在进行计算时一个题目多问时,尽可能的在同一个化学方程式中来解答.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 汤内盐的质量分数随着水分蒸发而增大 | |
| B. | 汤的上部淡下部咸 | |
| C. | 汤内锅底的盐没溶解 | |
| D. | 其它原因 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
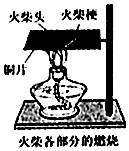
| A. | 有可燃物 | B. | 有助燃剂 | ||
| C. | 温度达到可燃物的着火点 | D. | 可燃物与火焰直接接触 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 复分解反应 | B. | 化合反应 | C. | 分解反应 | D. | 置换反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com