

| A. | 步骤Ⅰ通过一步反应即可实现 | |
| B. | 步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁 | |
| C. | 步骤Ⅴ中化学能转化为电能 | |
| D. | 该流程涉及的基本反应类型有4种 |
分析 高温条件下碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,氢氧化钙和氯化镁反应生成氢氧化镁沉淀和氯化钙,氢氧化镁和稀盐酸反应生成氯化镁和水,电解氯化镁生成镁和氯气,一定条件下氢气和氯气反应生成氯化氢,氯化氢溶于水形成盐酸.
解答 解:A、步骤Ⅰ是通过两步反应实现的,即碳酸钙分解生成氧化钙和二氧化碳,氧化钙和水反应生成氢氧化钙,该选项说法不正确;
B、步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁,该选项说法正确;
C、步骤Ⅴ中电能转化为化学能,该选项说法不正确;
D、该流程涉及的基本反应类型有分解反应(碳酸钙分解生成氧化钙和二氧化碳)、化合反应(水和氧化钙反应生成氢氧化钙)、复分解反应(例如氯化镁和氢氧化钙反应生成氢氧化镁沉淀和氯化钙)等3种,不包括置换反应,该选项说法不正确.
故选:B.
点评 本题主要考查物质的性质,解答时要根据各种物质的性质,结合各方面条件进行分析、判断,从而得出正确的结论.


科目:初中化学 来源: 题型:选择题
| A. | 硫酸盐 | B. | 碳酸盐 | C. | 二氧化碳 | D. | 硝酸盐 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
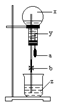 如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )
如图所示,烧瓶内充有x气体,若挤压滴管的胶头a,使液体y进入烧瓶中,振荡烧瓶,并倒放在铁架台上,将导管伸入滴有z的水中,打开弹簧夹b,可见烧杯中液体如喷泉一样喷入烧瓶中,并出现颜色的改变,则x、y、z可能是( )| x气体 | y液 | z试剂 | |
| ① | O2 | H2SO4 | 紫色石蕊试液 |
| ② | CO2 | NaOH | 无色酚酞试液 |
| ③ | CO | Ca(OH)2 | 无色酚酞试液 |
| ④ | HCl | H2O | 紫色石蕊试液 |
| A. | ②④ | B. | 只有② | C. | ①② | D. | ③④ |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 加入稀盐酸的次序 | 1 | 2 | 3 | 4 |
| 加入稀盐酸的质量(克) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(克) | 4.0 | m | 1.2 | 1.2 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
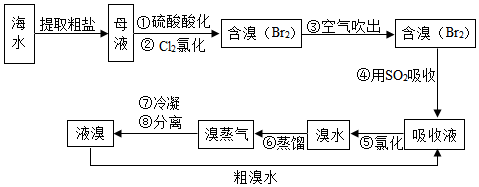
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
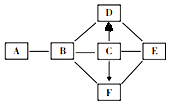
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 二氧化氯(ClO2)1000毫升 | |
| 溶质的质量分数 | 80% |
| 密度 | 1.2克/厘米3 |
| 强腐蚀性,阴冷,密封储藏 | |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com