
【题目】下列应用和相应的原理(用化学方程式表示)及基本反应类型都正确的是()
A. 用过氧化氢溶液和二氧化锰制氧气2H2O2![]() 2H2O+O2↑ 分解反应
2H2O+O2↑ 分解反应
B. 用天然气作燃料CH4+2O2![]() CO2+2H2O 氧化反应
CO2+2H2O 氧化反应
C. 用铁制容器盛放稀盐酸Fe+2HCl═FeCl2+H2↑ 置换反应
D. 用熟石灰制生石灰CaO+H2O═Ca(OH)2 化合反应
科目:初中化学 来源: 题型:
【题目】已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:
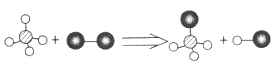
则下列说法中正确的是
A. 图示中的反应物都是化合物 B. 该反应属于化合反应
C. 该反应中的四种物质中可能有氧化物 D. 该图示符合质量守恒定律
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】为了探究碱的化学性质,同学们进行了如图所示的实验。
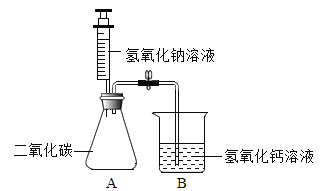
(实验操作)
夹紧弹簧夹,将注射器中的氢氧化钠溶液全部注入锥形瓶中。锥形瓶中发生反应的化学方程式为_____。反应一段时间后,打开弹簧夹,观察到的现象为_____,锥形瓶底部有白色沉淀生成。
(废液处理)
(1)将反应后锥形瓶内的物质全部倒入烧杯B中,然后滴入几滴无色酚酞溶液,充分混合后,烧杯内的液体为_____色。
(2)再向烧杯中倒入一定量的稀盐酸,充分反应后,烧杯内得到无色澄清溶液,则该无色溶液中一定含有的溶质是_____。请写出该烧杯内发生中和反应的化学方程式_____(写一个)。
(3)最后烧杯内的无色溶液能否直接排放,请阐述你的观点并说明理由_____。
(反思交流)上述实验活动验证了碱可以与某些物质发生化学反应。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。下列说法中正确的是
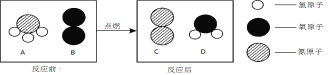
A. 该反应前后原子和分子种类均不变B. 该反应属于置换反应
C. A中氮元素的化合价为-3价D. 参加反应的A和B的质量比为17∶32
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】2018年1月11日,广西某地高速公路大桥上用于融冰作业的2包共100公斤含有亚硝酸钠的工业盐遗失,当地迅速组织警力开展搜寻遗失的工业盐,确保不流入市场和家庭。
(资料卡1)亚硝酸钠与食盐氯化钠相似,为白色有咸味的固体,但误食会使人中毒。腌制食品、泡菜等制作过程中会产生亚硝酸钠。
根据以上资料,回答下列问题:
(1)用盐融冰的原理是____,该过程主要发生的是___(填“物理变化”或“化学变化”)。
(2)下图是用不同浓度盐水腌制泡菜过程中亚硝酸盐含量测定曲线图。据此回答:当盐水浓度为6%时,第____天亚硝酸盐含量达到最大值。为了安全,泡菜腌制时盐水浓度最好是____并在腌制____天后再食用。
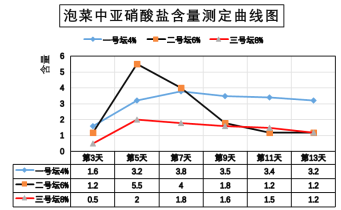
(3)兴趣小组欲测定某工业盐中亚硝酸钠的质量分数
(资料卡2)实验室常用亚硝酸钠与氯化铵溶液反应制取纯净的氮气,其化学方程式为:NaNO2 + NH4Cl ![]() NaCl + N2↑+ 2H2O(此反应是放热反应)
NaCl + N2↑+ 2H2O(此反应是放热反应)
(资料卡3)在酸性环境中高锰酸钾能与亚硝酸钠发生如下反应:2KMnO4 + 5NaNO2 + 3H2SO4 = K2SO4 + 2MnSO4 + 5NaNO3 + 3H2O
(方案一)取1g该工业盐样品与足量氯化铵溶液于如图装置中充分反应(该工业盐中其他成分不与氯化铵溶液反应),实验时加热片刻后,即可移去酒精灯,其原因___。最终量筒中收集到300mL水,已知该条件下氮气的密度为1.25g/L,则该工业盐样品中亚硝酸钠的质量分数为____(写出计算过程,结果保留一位小数,)。
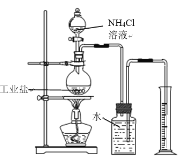
实验结束后发现测量结果偏大,可能原因是____。
(方案二)为更准确地测定该工业盐中亚硝酸钠的含量,称取4.000g样品溶于水配成250mL溶液,取25.00mL溶液于锥形瓶中,用含量为15.8g/L的酸性KMnO4溶液进行反应,实验所得数据如下表所示:
实验次序 | 1 | 2 | 3 | 4 |
KMnO4溶液体积(mL) | 20.60 | 20.02 | 20.00 | 19.98 |
上述第____次实验所得数据明显异常,剔除异常数据后,计算出该工业盐中亚硝酸钠的质量分数为___。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】根据如图A、B、C三种固体的溶解度曲线回答:

(1)20℃时,欲配制等质量的A、B两种物质的饱和溶液,所需水的质量关系是A________B(填写“>”、“<”或“=”).
(2)要在不改变溶质的质量分数的前提下使50℃时C的饱和溶液成为不饱和溶液,可采用的方法是________.
(3)将50℃时三种物质的饱和溶液分别都降温到20℃,此时溶液中溶质的质量分数从大到小是________.
(4)甲、乙两烧杯中分别装有50℃的100克和200克A的饱和溶液,若将两份溶液都降低到20℃,析出晶体质量的关系是甲________乙(填写“>”、“<”或“=”),若将两份溶液都恒温蒸发10克水,析出晶体质量的关系是甲________乙.
(5)欲从混有少量A的B物质的饱和溶液中得到纯净的B晶体,应该采用的方法是________.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】(1)地壳中含量最多的非金属元素是________。(写出元素符号)
(2)NH4NO3固体溶解过程________能量。(填“放出”或“吸收”)
(3)画出硫离子(S2-)的结构示意图________。
(4)打开盛有浓盐酸的试剂瓶会看到瓶口出现________。
(5)向滴加两滴酚酞试剂的氢氧化钠溶液中,逐滴滴加稀硫酸至过量,可观察到的现象________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣活动小组为测定空气中氧气的含量,进行如下探究实验:

①实验中可以看到玻璃容器内白磷燃烧时的现象是_____,该反应的符号表达式是_____。实验结束后,恢复至常温,活塞应停在刻度_____处,出现该现象的原因是:_____。
②玻璃容器内余下的气体主要是_____。
③此反应中白磷要过量,目的是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图中的①、②分别是氯元素、钠元素在元素周期表中的信息,A、B、C、D是四种粒子的结构示意图.
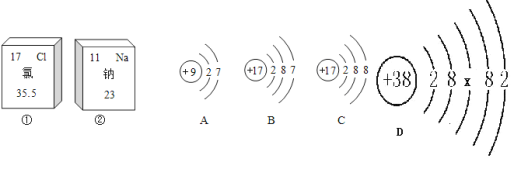
试回答下列问题:
(1)钠元素的原子序数为_____,画出它的原子结构示意图_____;
(2)A、B、C中属于同种元素的粒子是_____和_____;
(3)A和B两种粒子的_____相同,所以它们具有相似的化学性质;
(4)钠原子和氯原子反应所形成的化合物是由_____(填“分子”、“原子”、“离子”)构成的.
(5)如图D是锶(Sr)的原子结构示意图,则x的数值为:_____,锶元素的氧化物化学式为_____,通过如图分析可知,锶元素位于元素周期表的第_____周期.在同一周期中,原子的核外电子层数相同,从左至右_____依次递增.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com