
分析 (1)根据有关化学式的有关计算中的元素质量比的计算公式(即元素质量比=相对原子质量与相应原子个数的乘积比),来进行简单的计算即可;
(2)假设水的质量为x,根据所含的氢元素质量相等列出方程式,即可计算出41g角鲨烯与多少g水中所含的氢元素质量相等.
解答 解:(1)角鲨烯中碳、氢两元素的质量比为:(12×30):(1×50)=36:5;
(2)解:设水的质量为x,41g×$\frac{1×50}{410}$×100%=x×$\frac{1×2}{1×2+16}$×100%
x=45g.
答:角鲨烯的相对分子质量是410.41g角鲨烯与45g水中所含的氢元素质量相等.
故答案为:(1)36:5;(2)45g;
点评 本题主要考查学生运用化学式和元素的相对原子质量进行计算的能力.


科目:初中化学 来源: 题型:实验探究题
 查阅资料发现,氯化铵固体与亚硝酸钠固体混合加热也能制取氮气.反应的化学方程式如下:NH4Cl+NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2H2O+N2↑.
查阅资料发现,氯化铵固体与亚硝酸钠固体混合加热也能制取氮气.反应的化学方程式如下:NH4Cl+NaNO2$\frac{\underline{\;\;△\;\;}}{\;}$NaCl+2H2O+N2↑.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
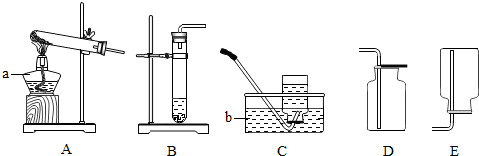
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 物质(杂质) | 操作方法 |
| A | CO2(H2O) | 将气体通过盛有火碱的干燥管 |
| B | Cu(CuO) | 通入足量氧气并加热 |
| C | FeCl2(CuCl2) | 加入足量铁屑,充分反应后过滤 |
| D | Na2SO4(Na2CO3) | 加盐酸至恰好不再产生气泡为止 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

| 加热时间(min) | 0 | t1 | t2 | t3 |
| 玻璃管及其中固体质量(g) | 56.66 | 55.20 | 54.80 | 54.80 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com