
����Ŀ��ij��ѧС��������ϳ���̽������֪�����ȵ�����غ��Ȼ��ƵĻ�������ᴿ���������
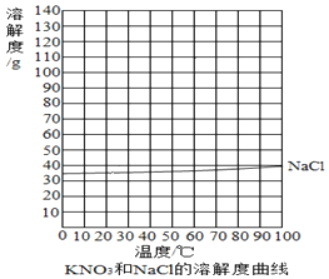
�������ᴿ������
����غ��Ȼ����ڲ�ͬ�¶�ʱ���ܽ��
�¶�/�� | 0 | 20 | 40 | 60 | 80 | 100 | |
�ܽ��/g | KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 | |
��1��20��ʱ��NaCl���ܽ��Ϊ_____�� ��20g NaCl����50gˮ�����Ƴ�_____g NaCl��Һ��
��2�����ݱ������ݣ�����KNO3���ܽ������_____��
��3������KNO3���ܽ�����ߣ�Ԥ��KNO3��70��ʱ���ܽ��ԼΪ_____g��
������ᴿ���裩
��ѡȡ��Ʒ��85gKNO3��5gNaCl�Ļ���
������80��ʱKNO3�ı�����Һ����ˮԼ50mL��ˮ���ܶ�ԼΪ1gmL��1��
�۽�����20��
�ܵõ�����
������ᴿ������
��4��Ϊ��֤�� ���еõ��ľ���Ϊ������KNO3����С��ͬѧ�������֪ʶ���������ϳ�����������·������������Dz�ͬ���ʶ��ܽ�ȵ��Ӱ�켰ʵ�������ˮ�������ʧ��Ӱ�����أ�
����һ ͨ����ѧʵ����м��飬ȡ�������еõ��ľ������Թ��У���ˮ�����Һ���μ�_____���۲�ʵ������û��_____��������NaCl��
������ ��������KNO3���������ԼΪ_____g����ȷ������������еõ�������������бȽϣ�����ȣ���NaCl��
���𰸡�36g 68 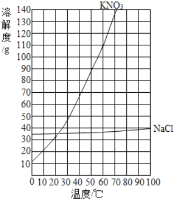 138 ������ ���� 77.2
138 ������ ���� 77.2
��������
��1��ͨ�������ܽ�����߿�֪��20��ʱ��NaCl���ܽ��Ϊ36g����20g NaCl����50gˮ�����Ƴ�68gNaCl��Һ��
��2�����ݱ�����������ڲ�ͬ�¶��µ��ܽ�ȣ��ú������ʾ�¶ȣ��������ʾ���ʵ��ܽ�ȣ��ɻ������ܽ���������£�
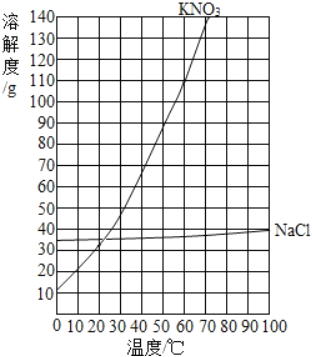
��3������KNO3���ܽ�����ߣ����KNO3��70��ʱ���ܽ��ԼΪ138g��
������ᴿ������
����һ ͨ����ѧʵ����м��飬ȡ������4���еõ��ľ������Թ��У���ˮ�����Һ���μ����������۲�ʵ������û�г�����������NaCl��
������ ��56.2gˮ��20��ʱ�ܽ�������Ϊx
100g��31.6g��56.2g��x
x��![]()
��������KNO3���������ԼΪ77.2g��


 ʱ�����������ҵԭ���ܳ�����ϵ�д�
ʱ�����������ҵԭ���ܳ�����ϵ�д� ����νӽ̲���ĩ���Ԥϰ�人������ϵ�д�
����νӽ̲���ĩ���Ԥϰ�人������ϵ�д� ������ҵ��ٳɳ����½������������ϵ�д�
������ҵ��ٳɳ����½������������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij���ֻ���·���к���Fe��Cu��Au��Ag��Ni(��������ɫ����)�Ƚ�����������ij�������ղ��ֽ���������ͼ����֪��2Cu+O2+2H2SO4![]() 2CuSO4+2H2O
2CuSO4+2H2O
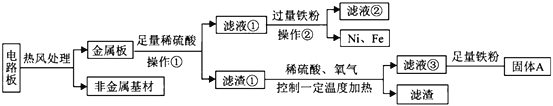
(1)�����ٵ�������____________________��
(2)д����Һ���н��������ӷ���____________________��
(3)д����Һ�ۺ����۷�����Ӧ��һ����ѧ����ʽ____________________________��
(4)Cu��Ag��Ni����Һ�еĻ����ǿ������˳��������____________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�������Ӫ���ɷֱ����(����̼ˮ��������Ҫָ���۵�)��
Ӫ���ɷֱ� |
��Ŀÿ100�� |
���� 1966ǧ�� ������ 7.5�� ֬�� 21.8�� ̼ˮ������ 60.7�� �� 2300���� |
(1)������������ָ_____(����ĸ���)��
A ����B ���� C Ԫ��D ����
(2)�÷������к���Ӫ������_____�֡�
(3)��������ʹ�õ�ʳ�ο����Ǽӵ��Σ�������ȱ����ܻ��еļ�����_____(������״���״�����������������)��
(4)������ͨ�����þ��������ϴ���װ�������������������ɫ��Ⱦ������������_____���ϡ�
(5)�й�������ʳָ�Ͻ���ÿ��ʳ��ʳ��ʯ����6�ˣ�����С��ij�����100�˸÷����棬�൱�ڳ���ʳ��_____�ˡ�(����С�����һλ)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʵ���Ҽ�������غͶ��������Ļ����28g��ȡ��������ȫ��Ӧ��ʣ���������Ϊ18.4g������㣺
��1������������������
��2��ԭ�����������ص�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ʵ�鷽������ܴﵽʵ��Ŀ���ǣ� ��
A. 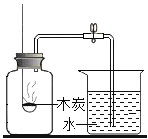 �ⶨ�����������ĺ���
�ⶨ�����������ĺ���
B. 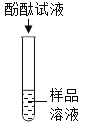 ����NaOH��Һ �Ƿ����
����NaOH��Һ �Ƿ����
C. 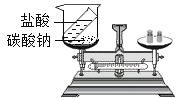 ��֤�����غ㶨��
��֤�����غ㶨��
D. 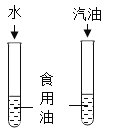 ̽��Ӱ�������ܽ��Ե�����
̽��Ӱ�������ܽ��Ե�����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ij����Ƭ�İ�װ�������汻һ�������ùĹĵġ�ij��ѧ��ȤС��ͬѧ�����������������Ȥ�������С��ͬѧһ��Ը��������̽����

��������⣩�������������ʲô�أ�
���������ϣ���ʳƷ�������Ӵ����ױ����������ܣ�
�����ij�������Է�����
���������裩������Ϊ�������������� ����Ϊ�������ǵ�����
����Ϊ�������Ƕ�����̼�� ����Ϊ��������������
���������ۣ���
С��ͬѧ��������һ����Ϊ�IJ��벻��ȷ��������_____��
�����䡢���氲ȫ�Ƕȿ��ǣ�_____ͬѧ����Ҳ�����ܡ�
��ʵ����ƣ���Ϊ̽��������룬С��ͬѧ�������ʵ�飬����д�հף�
ʵ�鲽�� | ʵ������ | ʵ����� |
��ע������ȡ���ڵ����壬Ȼ��ע�����ʯ��ˮ�� | �����Ա仯 | ������ȷ |
_____ | ��������ȷ |
����˼��չ����ʵ���С��ͬѧ��Ϊ��ΪʳƷ�ķ����������ѧ���ʲ����ã�����ʳƷ��Ӧ�⣬��Ӧ�߱�ijЩҪ������ΪӦ�þ߱���ЩҪ����һ�㣩_____��
����Ϊ�������װʳƷ�����������⣬������_____���á�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ͬѧ����Na2CO3��Һ��ŨHCl���о�����������ķ�Ӧԭ��ʱ���Է�Һ�ijɷֽ���̽����
���������裩�����������ʷ�����Ӧ�Ļ�ѧ����ʽΪ��_____���ɴ��Ʋ����Һ��һ����NaCl��������Na2CO3�����ᡣ
��ʵ��̽����
��1��ȷ����Һ���Ƿ������
��ѡ���Լ�����������Ļ�ѧ���ʣ�ͬѧ��ѡ������ͼ����ʾ���������ʣ���������X�����ָʾ���е�_____��Һ��
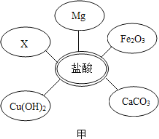
��ʵ����֤��ijͬѧ���Һ�м���������þ�ۣ��۲쵽_____��ȷ����Һ��һ��û�����ᡣ
��2��ȷ����Һ���Ƿ���Na2CO3��ijͬѧѡ��_____�����Һ��pH��l0��
ȷ����Һ��һ������Na2CO3��
��3��������Һ���������ã����ӷ�Һ�еõ�������NaCl�����������ʵ�鷽����ơ�
���� | �����Լ� | ���뷽�� | �������� |
һ | ����Ca��NO3��2��Һ | ���ˡ������ᾧ | �����У������ǣ�_____ |
�� | �Թ�����_____ | _____ | ���� |
��4����չ���ã�
��ͼ�ҷ�������BaCl2��NaCl�Ĺ�������ʱ��X��Һ��������_____��
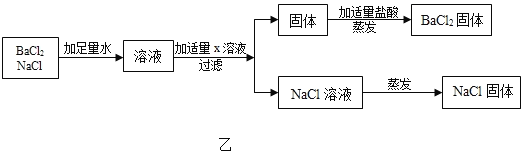
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ɱ�����(C3H7NO2)�ȶ��ְ����ṹ�ɵġ����ݱ�����Ļ�ѧʽ���㣺
(1)��������_____��Ԫ����ɣ�
(2)���������Է�������Ϊ_____��
(3)�������е�����Ԫ�ص�������Ϊ_____��
(4)̼Ԫ�ص�����������_____(��ȷ��0.1%)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijУѧϰС����̽������IJⶨ�����ݴ���������
��������⡿
�������ʯ��ʯ����Ҫ�ɷ�ΪCaC03����ϡ���ᷴӦ���ⶨ����CO2����������������������ݡ�
��ʵ����ơ�ͨ����������ʵ��ֱ�ⶨC02�������������

����������
��1�� ʵ��I�У���С�ձ��е�����ϡ����ּ��μ��뵽���ձ��У������Ͻ��裬�ж�ʯ��ʯ��CaC03��ȫ��Ӧ��ʵ�������� ��
��2�� ʵ�����У������Ӻ�װ�ò���������ԣ�Ȼ��װ��ҩƷ�����10 mLϡ�������������ƿ�С���ϡ�����Ƿּ��λ�������ģ��������ɵĺ���� ��
����¼�봦����
��3�� ��֪ʵ��I��Ӧǰ��������[m�����ձ�ʮʯ��ʯ��ĩ��+m��С�ձ�ʮϡ���ᣩ]��Ҫ��������C02�����������ٻ���Ҫ��������
A��m��С�ձ��� B��m(���ձ�) C��m(���ձ�ʮ��Ӧ��ʣ����)
��4�� ʵ������ʵ���¼���£�������������ͬ�¶ȡ���ͬѹǿ�����²ⶨ����

��������ʵ����̺������ۺϷ�������������C02����� mL��
��5�� ��ѧϰС���ͬѧ�ɼ���һ��ʯ��ʯ��Ʒ����������Ƴ�6g�����ձ��ڣ��ձ�����Ϊ20 g����Ȼ�����50 gϡ���ᣨ����������ַ�Ӧ���ٳ���Ϊ73.8 g�����ձ�һ�𣩡��Իش�
����ʯ��ʯ��Ʒ�������ҪĿ���� ��
����ʵ������У�������CO2������ ��
����ʯ��ʯ��Ʒ��̼��Ƶ����������Ƕ��٣���д��������̣��������һλС����
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com