


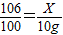 解得X=10.6g,根据:
解得X=10.6g,根据: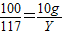 解得Y=11.7g
解得Y=11.7g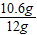 ×100%=88.3%;
×100%=88.3%;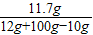 ×100%=11.47%
×100%=11.47%

科目:初中化学 来源: 题型:阅读理解
氢氧化钠(溶液) 氢氧化钠(溶液) |
10% 10% |
查看答案和解析>>
科目:初中化学 来源: 题型:
| ||
| ||
| ||
| ||
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

| 方案 | 选用的药品 | 选用的实验装置及组装时接口连接顺序 | 需测得的实验数据(从上述可测得的数据中选取) | 混合物中Na2CO3的质量分数计算式 | |||||
| 选用的实验装置序号 | 组装时接口编号顺序 | ||||||||
| 一 | CaCl2溶液 CaCl2溶液 |
A、B、D、F | (毋须填写) | ag、bg ag、bg |
| ||||
| 二 | 稀H2SO4 稀H2SO4 |
A、C、E A、C、E |
①④⑤②③ ①④⑤②③ |
ag、cg、dg |
| ||||
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解

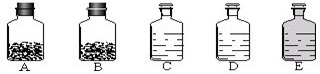
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com