

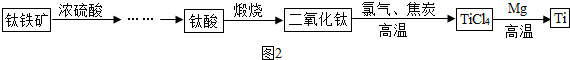
分析 (1)根据反应的原理来分析;
(2)根据化学方程式的书写方法填写化学方程式,根据反应类型的特点判断反应类型;
(3)根据金属活动性顺序表进行分析,在金属活动性顺序中,排在氢前面的金属能与酸反应生成氢气,位置在前的金属能将位于其后的金属从其盐溶液中置换出来;
(4)根据硫酸铜的质量求出参加反应铁的质量和生成铜的质量,从而求出含杂质的铁的质量是进行解答.
解答 解:(1)焦炭在高炉中主要是提供能量及得到还原剂,高炉内的反应需要热量也是需要焦炭提供;二氧化碳与焦炭在高温下反应生成一氧化碳;故填:提供热量和生成还原剂;C+CO2$\frac{\underline{\;高温\;}}{\;}$2CO;
(2)TiCl4与Mg反应的反应物是TiCl4与Mg,生成物是Ti和MgCl2,因此该反应的化学方程式是TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$Ti+2MgCl2;该反应中TiCl4、MgCl2是化合物,Ti、Mg是单质,属于一种单质和一种化合物反应生成另外一种单质和另外一种化合物的反应,是置换反应;反应需在氩气环境中进行,是因为氩气的化学性质稳定,可做保护气;故填:TiCl4+2Mg$\frac{\underline{\;800℃\;}}{\;}$Ti+2MgCl2;置换;防止高温条件下镁和钛被氧化;
(3)根据金属活动顺序表可知,锌比铁活泼,铁比铜活泼,所以加入一定量的锌粉,首先锌粉和硫酸铜溶液反应,置换出单质铜,锌会与稀硫酸反应生成硫酸锌,如果锌粉足量可以继续与硫酸亚铁反应置换出铁,由题意可知,向滤出的固体中滴加盐酸,有气泡产生,说明固体中含有和稀硫酸反应的金属,由题可知,金属可能是铁或铁和锌,锌会与硫酸铜反应生成硫酸锌和铜,所以滤渣和滤液中一定含有的物质是:铜和铁,硫酸锌.
故答案为:Fe和Cu;ZnSO4;
(4)解:设:样品中铁的质量为x,生成铜的质量为y,
硫酸铜的质量=160g×10%=16g
Fe+CuSO4=FeSO4+Cu
56 160 64
x 16g y
$\frac{56}{160}=\frac{x}{16g}$
x=5.6g
$\frac{160}{64}=\frac{16g}{y}$
y=6.4g
含杂质的铁的质量是5.6g+(6.8g-6.4g)=6g
则铁的质量分数为:$\frac{5.6}{6g}×100%$≈93.3%
点评 掌握化学方程式的计算格式和规范性,本题的难点是分析固体的成分的计算,一定要考虑杂质的质量.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:填空题
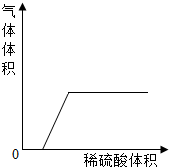 从HCl、NaCl、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合,可能得到澄清溶液的组合有许多种.
从HCl、NaCl、NaOH、Na2CO3、Ca(OH)2几种溶液中取出其中的两种混合,可能得到澄清溶液的组合有许多种.查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| A. | 1:1 | B. | 1:2 | C. | 3:4 | D. | 3:8 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
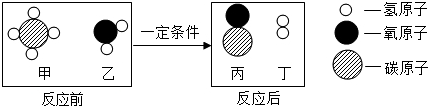
| A. | 反应前后分子个数不变 | |
| B. | 生成物丙中各元素的质量比为1:1 | |
| C. | 生成的丙和丁的分子个数比为1:1 | |
| D. | 若有24g的甲参加反应,则生成丁的质量为9g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
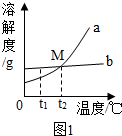 如图1是氯化钠和硝酸钾两种固体物质的溶解度曲线
如图1是氯化钠和硝酸钾两种固体物质的溶解度曲线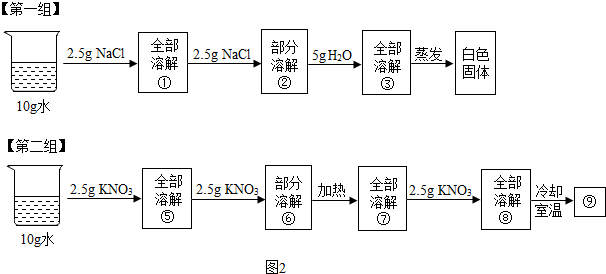
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com