
| A. | CaCO3和K2CO3 | B. | MgCO3和CaCO3 | C. | K2CO3和ZnCO3 | D. | ZnCO3和Ag2CO3 |
分析 首先根据碳酸钠和稀盐酸反应的化学方程式计算可分析出,如果是纯的碳酸钠和稀盐酸反应,生成4.4g二氧化碳消耗的碳酸钠恰好是10.6g,所以碳酸钠中含有的两种杂质如果分别也是10.6g,那么它们各自和稀盐酸反应产生的二氧化碳的质量必须是一个大于4.4g,一个小于4.4g,那么平均结果才可能等于4.4g.
解答 解:A、10.6g碳酸钾和稀盐酸反应产生的二氧化碳小于4.4g,而10.6g碳酸钙和稀盐酸反应产生的二氧化碳大于4.4g,所以碳酸钠中如果含有碳酸钾和碳酸钙,产生的二氧化碳可能等于4.4g.故正确;
B、10.6g碳酸镁和稀盐酸反应产生的二氧化碳质量大于4.4g,而10.6g碳酸钙和稀盐酸反应产生的二氧化碳的质量也大于4.4g,所以10.6g不纯的碳酸钠中如果含有碳酸镁和碳酸钙的话,和稀盐酸反应产生的二氧化碳不可能等于4.4g.故错误;
C、10.6g碳酸钾和稀盐酸反应产生的二氧化碳小于4.4g,而10.6g碳酸锌和稀盐酸反应产生的二氧化碳也小于4.4g,所以碳酸钠中不可能含有碳酸钾和碳酸锌.故错误;
D、10.6g碳酸锌和稀盐酸反应产生的二氧化碳也小于4.4g,10.6g碳酸银和稀盐酸反应产生的二氧化碳小于4.4g,所以碳酸钠中不可能含有碳酸锌和碳酸银.故错误;
故选A.
点评 此题是利用不纯的物质和酸反应产生的气体的质量来判断此不纯的物质可能含有的杂质,而极端分析法是做此题常用的方法,同学们如果掌握了这个方法就可以解决这一类问题.


 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:初中化学 来源: 题型:选择题
| A. | 青蒿素分子由三种元素组成 | B. | 青蒿素是一种有机物 | ||
| C. | 青蒿素含有42个原子 | D. | 青蒿素中氢元素的质量分数最大 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
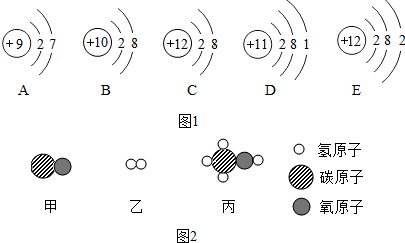
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 酸雨的形成:CO2+H2O═H2CO3 | |
| B. | 盐酸除铁锈:Fe2O3+6HCl═2FeCl3+3H2O | |
| C. | 铁丝在氧气中燃烧:3Fe+2O2$\frac{\underline{\;点燃\;}}{\;}$Fe3O4 | |
| D. | 用烧碱溶液吸收二氧化硫:2NaOH+SO2═Na2SO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 碱:纯碱、熟石灰、氨水 | B. | 有机物:甲烷、乙醇、醋酸 | ||
| C. | 合金:合成纤维、铝合金、玻璃钢 | D. | 混合物:水煤气、碘酒、冰水混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用食醋可除去水壶内壁的水垢 | |
| B. | 用淬火处理过的缝衣钢针可制钓鱼钩 | |
| C. | 用汽油可清洗衣服上的油渍 | |
| D. | 用互刻画的方法可确定铜与黄铜的硬度 |
查看答案和解析>>
科目:初中化学 来源: 题型:多选题
| 物质 | 所含杂质 | 除去杂质的方法 | |
| A | CO2 | HCl | 通过饱和NaHCO3溶液和浓硫酸 |
| B | NaCl溶液 | Na2SO4溶液 | 加入适量的硝酸钡溶液,过滤 |
| C | MnO2 | KCl | 加水充分溶解,过滤、蒸发结晶 |
| D | NaOH溶液 | Ca(OH)2溶液 | 加入适量碳酸钠溶液,过滤 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
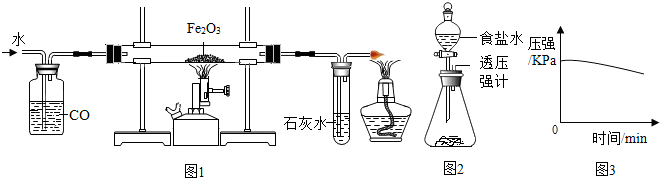
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com