
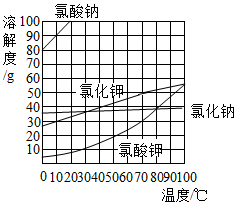
 根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )
根据如图提供的几种物质的溶解度曲线,判断下列说法正确的是( )| A. | 氯酸钾中混有少量氯化钠,提纯氯酸钾最好用蒸发结晶的方法 | |
| B. | 30℃氯酸钾饱和溶液的溶质质量分数为10% | |
| C. | 80℃时7gNaCl和20g水能形成饱和溶液 | |
| D. | 控制温度,图中氯酸钠和氯化钾能发生化学反应 |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、氯酸钾的溶解度受温度变化影响较大,所以氯酸钾中混有少量氯化钠,提纯氯酸钾最好用降温结晶的方法,故A错误;
B、30℃时,氯酸钾的溶解度是10g,所以氯酸钾饱和溶液的溶质质量分数为:$\frac{10g}{100g+10g}$×100%=9.1%,故B错误;
C、80℃时7g氯化钠在20g水中形成饱和溶液也就是80℃时溶解度为35g,而从图上可以明显看出80℃时氯化钠的溶解度大于35g,故C错误;
D、氯酸钠和氯化钾交换成分可以得到氯酸钾和氯化钠,这个反应是一个复分解反应,但是很明显它不符合初中阶段所学的复分解反应发生的条件,控制温度在10-30℃之间,氯化钠的溶解度较大,氯酸钾的溶解度较小,会以晶体形式析出,所以图中氯酸钠和氯化钾能发生化学反应,故D正确.
故选:D.
点评 本题难度比较大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.


 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案 小学暑假作业东南大学出版社系列答案
小学暑假作业东南大学出版社系列答案 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 芬太奴的每一个分子中含有47个原子 | |
| B. | 芬太奴是由碳、氢、氧、氮四种元素组成的物质 | |
| C. | 芬太奴中碳的质量分数最大 | |
| D. | 芬太奴中碳、氢、氧、氮的原子个数比为240:24:28:16 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
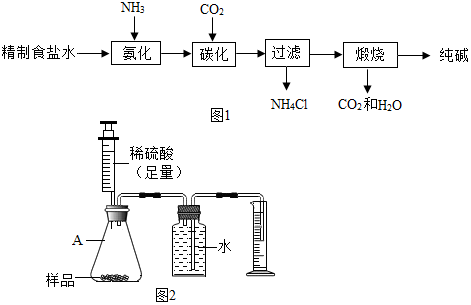
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com