
 某溶液可能由硝酸、氯化钠、硫酸钠、氯化铜溶液中的一种或几种混合而成.为探究其组成,小明进行了如下实验:
某溶液可能由硝酸、氯化钠、硫酸钠、氯化铜溶液中的一种或几种混合而成.为探究其组成,小明进行了如下实验:

科目:初中化学 来源: 题型:
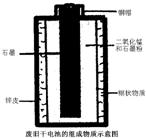 (2007?青岛)下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,
(2007?青岛)下面是某化学兴趣小组探究废旧干电池中白色糊状物成分的过程,| 实验操作 | 实验现象 | 实验结论 |
| (1)取糊状物少量,加足量的水,搅拌后过滤.取少量滤液于试管中,滴加硝酸钡溶液. | 没有沉淀生成 没有沉淀生成 | 没有SO42-和CO32-存在 |
| (2)另取第(1)不所得滤液少量,滴加少量 硝酸银 硝酸银 溶液 | 产生白色沉淀 | 存在的离子是 氯离子 氯离子 |
| (3)取白色糊状物,滴加少量 碘 碘 溶液 | 出现蓝色 | 有淀粉存在 |
查看答案和解析>>
科目:初中化学 来源: 题型:

查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
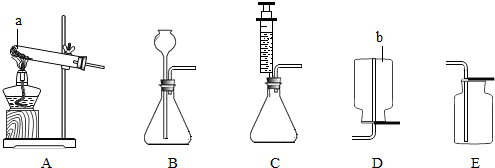
| ||
| △ |
| ||
| △ |
| 猜想 | 主要操作 | 主要现象 | 实验结论 |
| 猜想一 | 打磨R丝,并将其插入到硫酸铜溶液中 | R丝表面覆盖了一层红色的物质 | 猜想一 不成立 不成立 (填“成立”或“不成立”) |
| 猜想二 | 打磨粗细相同的R丝、铝丝、铜丝,分别将它们插入到体积相同、溶质质量分数也相同的稀硫酸中 | ①R丝表面产生气泡缓慢,溶液由无色逐渐变成蓝色 ②铝丝表面产生气泡较快 ③铜丝表面没有气泡产生 |
猜想二成立. R与稀硫酸反应的化学方程式为 R+H2SO4═RSO4+H2↑ R+H2SO4═RSO4+H2↑ |
| 猜想三 | 将打磨过的铝丝插入到RSO4[或RCl2或R(NO3)2]溶液中 将打磨过的铝丝插入到RSO4[或RCl2或R(NO3)2]溶液中 |
无明显现象 | 猜想三成立 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com