
| 实 验 步 骤 | 实验现象 | 实验结论 |
| 1.取少量的污水,仔细观察. | 溶液呈无色、透明、不沉淀 | 没有Fe3+ |
| 2.①将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较 | pH试纸呈深蓝色 | 溶液的pH=13 |
| 3.取2毫升的污水,滴入稀硫酸溶液 | ②产生白色沉淀 | 污水中含有Ba2+ |
分析 (1)根据测定溶液pH具体操作步骤写出实验步骤即可,根据硫酸根离子遇到钡离子,生成硫酸钡白色沉淀考虑本题;(2)溶液呈无色、透明、不沉淀,说明没有Fe3+;pH试纸呈深蓝色,溶液的pH=13说明溶液显碱性,即含有OH-;滴入稀硫酸溶液,产生白色沉淀,说明含有Ba2+.根据溶液中离子共存的原理,含有钡离子,就一定不含硫酸根离子.再进行分析即可.
解答 解:(1)测定溶液pH具体操作步骤:将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较,就能测出pH值,硫酸根离子遇到钡离子,生成硫酸钡白色沉淀,所以现象是产生白色沉淀;
(2)溶液呈无色、透明、不沉淀,说明没有Fe3+;pH试纸呈深蓝色,溶液的pH=13说明溶液显碱性,即含有OH-;滴入稀硫酸溶液,产生白色沉淀,说明含有Ba2+.溶液中离子必须能够共存的原理,含有钡离子,就一定不含硫酸根离子.所以一定含有的污染物是氢氧化钡.
故答案为:(1)
| 实 验 步 骤 | 实验现象 | 实验结论 |
| 1.取少量的污水,仔细观察. | 溶液呈无色、透明、不沉淀 | 没有Fe3+ |
| 2.①将一片pH试纸放在玻璃片上,用玻璃棒蘸取待测液滴到pH试纸上,将试纸呈现的颜色与标准比色卡比较 | pH试纸呈深蓝色 | 溶液的pH=13 |
| 3.取2毫升的污水,滴入稀硫酸溶液 | ②产生白色沉淀 | 污水中含有Ba2+ |
点评 解答本题关键是知道铁离子溶液是黄色,熟悉离子共存问题,离子相互结合不能产生沉淀、气体或水.


科目:初中化学 来源: 题型:选择题
| A. | ①② | B. | ③④ | C. | ①②⑤ | D. | ③⑤⑥ |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
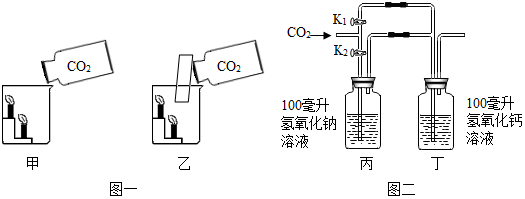
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 2.1g | B. | 2.4 g | C. | 3.6g | D. | 8.4g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | -1 | B. | +1 | C. | +3 | D. | +5 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 洒在桌面上的酒精燃烧起来,立即用湿抹布或沙子盖灭 | |
| B. | 浓硫酸不小心溅到皮肤上,先用干布擦拭,接着用大量的水冲洗,再涂上3%~5%的小苏打溶液 | |
| C. | 误服氯化钡溶液,立即喝大量鲜牛奶或鸡蛋清 | |
| D. | 碱液洒在衣服上,用水冲洗后,再涂上硫酸溶液 |
查看答案和解析>>
科目:初中化学 来源: 题型:计算题
| 牙膏 | A | B | C |
| 摩擦剂 | 氢氧化铝 | 碳酸钙 | 二氧化硅 |
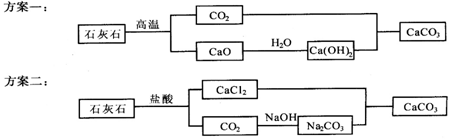
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 物质名称 | 乙烷 | 丙烷 | 丁烷 | 戊烷 | 己烷 |
| 沸点/℃ | -88.6 | -42.2 | -0.5 | 36.1 | 69.2 |
| A. | 乙烷、丙烷和丁烷 | B. | 乙烷和丙烷 | C. | 只有己烷 | D. | 戊烷和己烷 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com