

分析 根据物质的溶解度曲线可以判断某一温度时物质的溶解度大小比较;
饱和溶液和不饱和溶液之间可以相互转化.
解答 解:(1)由物质的溶解度曲线可知,t2℃时,甲物质的溶解度是40g.
故填:40g.
(2)由物质的溶解度曲线可知,t1℃时,甲、乙、丙三种物质的溶解度由大到小的顺序是甲>乙>丙.
故填:甲>乙>丙.
(3)由物质的溶解度曲线可知,丙物质的溶解度随着温度的升高而减小,要使t1℃时接近饱和的丙溶液变成饱和溶液,可采用的方法有:升高温度,加入丙的固体,恒温蒸发溶剂等.
故填:升高温度.
点评 溶解度曲线能定量地表示出溶解度变化的规律,从溶解度曲线可以看出:同一溶质在不同温度下的溶解度不同;同一温度下,不同溶质的溶解度可能相同,也可能不同;温度对不同物质的溶解度影响不同.


 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:解答题


查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 族 周期 | ⅠA 1 | 0 18 | ||||||
| 1 | 1 H 氢 | ⅡA 2 | ⅢA 13 | ⅣA 14 | ⅤA 15 | ⅥA 16 | ⅦA 17 | 2 He 氦 |
| 2 | 3 Li 锂 | 4 Be 铍 | 5 B 硼 | 6 C 碳 | 7 N 氮 | 8 O 氧 | 9 F 氟 | 10 Ne 氖 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 在火炉旁放一盆水,防止煤气中毒 | |
| B. | 向食品袋中充入氮气,延长食品的保质期 | |
| C. | 做测定空气中氧气含量的实验时,用木炭代替红磷 | |
| D. | 实验室制CO2时,用稀硫酸代替稀盐酸和石灰石(大理石)反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
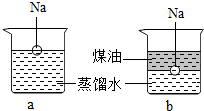 钠是一种非常活泼的金属,它能浮在水面上,与水面发生剧烈反应,反应放出的热量使钠熔化成小球,甚至会使钠和生成的氢气都发生燃烧;如图所示,把一块银白色的钠分别投入到水中和水与煤油里,在b中,钠同样与水发生剧烈反应生成氢氧化钠和氢气,但不发生燃烧.
钠是一种非常活泼的金属,它能浮在水面上,与水面发生剧烈反应,反应放出的热量使钠熔化成小球,甚至会使钠和生成的氢气都发生燃烧;如图所示,把一块银白色的钠分别投入到水中和水与煤油里,在b中,钠同样与水发生剧烈反应生成氢氧化钠和氢气,但不发生燃烧.查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com