
分析 (1)根据离子符号的写法以及原子核外的电子数来分析;
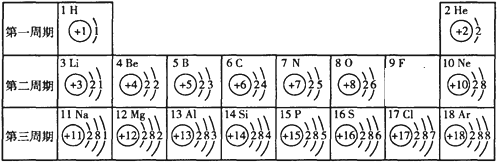
(2)根据元素周期表,从原子序数、核外电子数、电子层数等方面解答;
(3)根据元素在周期表中的信息和原子序数,质子数,核外电子数之间的关系及化合价的知识,解答本题.
(4)根据当质子数=核外电子数,为原子;当质子数>核外电子数,为阳离子;当质子数<核外电子数,为阴离子;决定元素的种类是核电荷数(即质子数),同种元素的粒子核电荷数(即质子数)相同;据此进行分析解答.
解答 解:( )氧原子和硫原子的最外层均为6个电子,易得到2个电子,而形成带两个单位负电荷的阴离子,故填:O2-(或S2-);
镁离子是由镁原子失去2个电子形成的,其核外有10个电子,与氖原子的核外电子排布相同,故填:氖;
(2)根据元素周期表中规律的知识可知元素周期表同一横行元素的排列规律是:在同一周期中,各原子的电子层数相同;同一周期中由金属逐渐过渡到非金属.
故答案为:在同一周期中,各原子的电子层数相同;同一周期中由金属逐渐过渡到非金属.
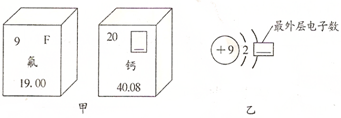
(3)①根据元素在周期表中的信息,图甲方框的横线上填的是钙元素的元素符号为Ca,在原子中,原子序数=质子数=核外电子数,根据题中元素的原子结构示意图,图乙方框横线上的数字是2+x=9,则x=7;故填:Ca;7;
②在化合物中,钙元素显+2价,氟元素显-1价,根据两种元素化合价,形成化合物的化学式为CaF2,故填:CaF2.
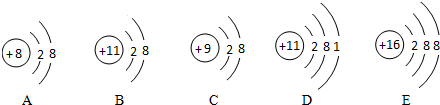
(4)A、质子数=8<核外电子数=10,为阴离子; B、质子数=11>核外电子数=10,为阳离子;
C、质子数=9<核外电子数=10,为阴离子; D、质子数=核外电子数=11,为原子;
E、质子数=16<核外电子数=18,为阴离子;
根据决定元素的种类是核电荷数(或质子数),由粒子结构示意图可知:BD中的质子数相同,因此属于同种元素的粒子是BD.
故答案为:D;B;ACE;BD.
点评 本题考查学生根据原子结构示意图分析总结元素周期律及对元素的性质与最外层电子数的关系的理解与掌握,并能在解题中灵活应用.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 水在通常情况下是无色、无味的液体 | |
| B. | 铜在潮湿的空气中表面会生铜绿 | |
| C. | 将甘蔗榨成甘蔗汁 | |
| D. | 将记录有机密信息的纸张粉碎 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C、H、S元素质量比为6:10:3 | B. | 由三种元素组成 | ||
| C. | 一个分子中含有六个硫原子 | D. | 相对分子质量为178g |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 减少药品 | B. | 减少砝码或移游码 | ||
| C. | 调节天平的平衡螺母 | D. | 增加药品 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 自然界中产生氧气的途径主要是植物的光合作用 | |
| B. | “氧循环”指得是氧气的循环,多是物理变化 | |
| C. | 对于相对稳定的大气来说“氧循环”有没有无所谓 | |
| D. | 物质在空气中的缓慢氧化是释放氧气的过程 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 固体NaOH会挥发 | |
| B. | 固体NaOH容易吸收空气中的水分而潮解 | |
| C. | 固体NaOH受热或光照会分解 | |
| D. | 固体NaOH会被空气中的氧气氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com