
| 反应前 | 反应后 |  | ||
| A | B | C | D | |
 | 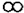 |  |  | |
分析 (1)根据燃气灶中的钢火圈是金属材料,塑料旋钮是有机合成材料,燃气燃烧不完全会产生炭黑,需要增大氧气的进量进行分析.
(2)①由图可以看出:相同质量的三种物质燃烧时,其中煤燃烧时产生的二氧化硫气体最多;天然气燃烧时产生的二氧化碳和二氧化硫最少去分析;
②氧化物是只含有两种元素且其中一种元素是氧元素的化合物,结合图示判断各物质的分子构成,进行分析判断.
由质量守恒定律可知,化学反应前后原子的种类、数目不变,确定参加反应的A、B、C、D四种分子的个数比,书写反应的方程式进而计算出A和C的质量比.
(3)对比结合图丙的表示元素质量分数的方法,利用甲烷的化学式计算出甲烷中碳、氢元素的质量之比就可采用丁图示表示各元素质量分数的关系;
(4)①磷酸二氢铵在受热时,能够生成氨气、水、五氧化二磷,同时吸收大量的热,据此写出化学反应方程式;②可根据灭火原理来解答灭火球灭火过程中蕴含的原理;③根据常见化肥的常识解答.
解答 解:(1)燃气灶中的钢火圈是金属材料,塑料旋钮是有机合成材料,氧气的量不充足,燃气不能充分燃烧,燃气燃烧不完全会产生炭黑,需要增大氧气的进量,所以增大进风口.故填:塑料旋钮;氧气的量不充足,燃气不能充分燃烧;增大;
(2)①由图2可以看出:相同质量的三种物质燃烧时,其中煤燃烧时产生的二氧化硫气体最多,空气中的二氧化硫过多就会导致酸雨的形成;天然气燃烧时产生的二氧化碳和二氧化硫最少,所以对空气的影响也最小;故填:天然气;煤;
②据图可知,A和C都是由两种元素组成的纯净物,故B是单质,AC属于氧化物.根据反应和生成物的关系可以得出反应的化学方程式为 CO2+4H2═CH4+2H2O.该反应中A、C两种物质的质量比是(12+16×2):(12+1×4)=11:9;故填:AC;11:9;
(3)在甲烷中碳氧两种元素的质量比为:12:1×4=3:1,所以在丙图示中氢元素的质量分数应该占整个圆的四分之一,据此绘图即可;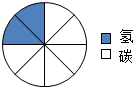 ;
;
(4)①依据磷酸二氢铵在受热时,能够生成氨气、水、五氧化二磷,同时吸收大量的热,写出磷酸二氢铵受热反应的化学方程式:2NH4H2PO4 $\frac{\underline{\;\;△\;\;}}{\;}$P2O5+2NH3↑+3H2O;故填:2NH4H2PO4 $\frac{\underline{\;\;△\;\;}}{\;}$P2O5+2NH3↑+3H2O;
②阅读:“火立熄”灭火球是一种新型灭火装置,在受到球体中心膨破力倒能将球体内的灭火干粉均匀爆撒开,附着在可燃物的表面,使其达到灭火效果.可回答该灭火球灭火过程中蕴含的原理之一是隔绝氧气;故填:隔绝氧气;
③根据常见化肥的常识可知:A、磷酸二氢铵还是一种常用的化肥,选项正确;B.磷酸二氢铵属酸式盐,使用该化肥时应避免与碱性物质混用,选项正确;C.通过计算知:该化肥中氢、氧元素质量比为(1×6):(16×4)=3:32;故该选项错误;D.运输、储存该化肥时应避免日晒雨淋,选项正确.说法不正确的是:C.
点评 本题难度不大,在能源危机和全球变暖日益严峻的背景下,节能减排、新能源的开发和利用势在必行,同时也是中考的热点.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 结论 |
| 先用pH试纸测定稀盐酸的pH,再逐渐滴加氢氧化钠溶液.并不断振荡,同时测定混合液的pH. | pH逐渐变大, 最后pH≥7 | 稀盐酸与氢氧化钠 溶液能发生反应 |
| 实验步骤 | 实验现象 | 结论 |
| 稀盐酸与氢氧化钠 溶液反应放热 |
| 实验步骤 | 实验现象 | 结论 |
| 取少量上述反应后的溶液于试管中,滴加硫酸铜溶液 | 若生成蓝色沉淀 | 氢氧化钠溶液过量 |
| 若没有明显现象 | 稀盐酸与氢氧化钠溶液恰好完全反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 黄铜(Cu-Zn合金)可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20 g该样品向其中加入一定量的稀硫酸,恰好完全反应时,产生氢气的质量与加入稀硫酸的质量关系如图所示.请计算:(反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑)
黄铜(Cu-Zn合金)可以用来制造机器、电器零件及日用品.为了测定某黄铜样品中铜的质量分数,取20 g该样品向其中加入一定量的稀硫酸,恰好完全反应时,产生氢气的质量与加入稀硫酸的质量关系如图所示.请计算:(反应的化学方程式为Zn+H2SO4=ZnSO4+H2↑)查看答案和解析>>
科目:初中化学 来源: 题型:选择题
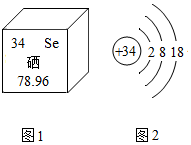 硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒元素的结构示意图,下列说法错误的是( )
硒对人体有防癌、抗癌作用,如图1是硒元素在元素周期表中的部分信息,图2是硒元素的结构示意图,下列说法错误的是( )| A. | 硒是人体必需的微量元素 | B. | 图2表示阴离子 | ||
| C. | 硒原子中子数是34 | D. | 硒是非金属元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 甲醛浸泡的海产品 | |
| B. | 霉变的大米、花生 | |
| C. | 用亚硝酸钠(NaNO2)代替食盐烹调的食品 | |
| D. | 食盐腌制的咸鸭蛋 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用肥皂水区别硬水和软水 | B. | 用水区别CaCO3和NaCl | ||
| C. | 用酚酞试液区别盐酸和食盐水 | D. | 用灼烧的方法区分羊毛和涤纶 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
 在哈尔滨市继今年1月份5台纯电动公交车上道试运营后,近日两台插电式气电混合动力公交车也在公交8路、107路上线试运营.插电式混合动力公交车车速23公里/小时以下,为纯电力驱动;速度超过23公里/小时,为气电混合驱动.按照测算,与常规天然气公交车相比,氮氧化物排放量可减少76%、二氧化碳排放量可减少60%,PM排放量可减少86%.回答下列问题.
在哈尔滨市继今年1月份5台纯电动公交车上道试运营后,近日两台插电式气电混合动力公交车也在公交8路、107路上线试运营.插电式混合动力公交车车速23公里/小时以下,为纯电力驱动;速度超过23公里/小时,为气电混合驱动.按照测算,与常规天然气公交车相比,氮氧化物排放量可减少76%、二氧化碳排放量可减少60%,PM排放量可减少86%.回答下列问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com