

分析 (1)由富马酸亚铁的化学式C4H2FeO4可知,它的相对分子质量=(碳的相对原子质量×碳原子个数)+(氢的相对原子质量×氢原子个数)+(铁的相对原子质量×铁原子个数)+(氧的相对原子质量×氧原子个数);
(2)根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析;
(3)根据2包补铁剂及每包含富马酸亚铁的质量及富马酸亚铁中铁元素的质量分数和硫酸亚铁中铁元素的质量分数来计算.
解答 解:(1)富马酸亚铁的相对分子质量为12×4+1×2+56+16×4=170,故填:170;
(2)富马酸亚铁中碳、氢元素的质量比为(12×4):(1×2)=24:1;故填:24:1;
(3)每天儿童最大用药量中含富马酸亚铁的质量为0.1g×3=0.3g=300mg,其中含铁元素:300mg×$\frac{56}{12×4+1×2+56+16×4}$×100%≈98.8mg=0.1g.
若要改服用FeSO4,为了达到同样的补铁效果,则每天需要服用FeSO4的质量为:0.1g÷$\frac{56}{56+32+16×4}×100%$=0.3g
故填:0.1;0.3.
点评 本题考查学生利用标签上物质的化学式进行简单计算,熟悉常见原子的相对原子质量即可计算解答.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
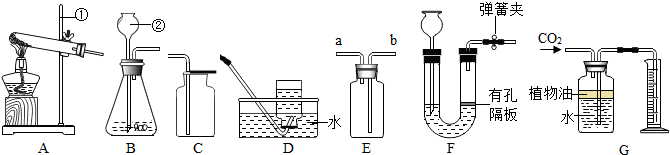
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
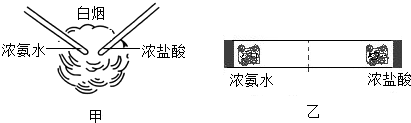
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氯气和一种气体单质.已知,在一个化学反应中,如有元素的化合价升高,同时必定有元素的化合价降低.则下列说法错误的是( )
如图是一种家用环保型消毒液发生器,其中发生的主要反应是氯化钠和水在通电条件下反应生成氢氧化钠、氯气和一种气体单质.已知,在一个化学反应中,如有元素的化合价升高,同时必定有元素的化合价降低.则下列说法错误的是( )| A. | 该反应是将电能转化为化学能 | |
| B. | 该发生器中产生的消毒剂可能是氯气 | |
| C. | 该反应中的未知气体单质一定是氢气 | |
| D. | 电解水实验中可加入氯化钠增强导电性 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com