
【题目】食盐是一种重要的化工原料,请回答下列问题。
(1)请完善实验室除去粗盐中泥沙等难容性杂质的实验步骤。![]()
①操作Ⅰ所用的玻璃仪器有:烧杯、玻璃棒和。
②蒸发过程中,待 时,停止加热,利用余热将滤液蒸干。
(2)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制,流程如图: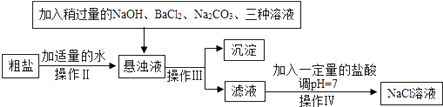
①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是(用化学方程式表示)。
②通过操作Ⅲ所得滤液中的溶质有(用化学式表示)。
(3)若有溶质质量分数为10%的氯化钠不饱和溶液100kg,要将其变成20℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是 。(已知:20℃时氯化钠的溶解度为36g。)
【答案】
(1)漏斗;蒸发皿中出现较多固体
(2)Na2CO3+BaCl2=BaCO3↓+2NaCl;NaOH、NaCl、Na2CO3
(3)加入22.4 kg的氯化钠固体
【解析】(1)①去除泥沙的步骤是:溶解:把粗盐放入烧杯中,加水溶解;过滤:架好漏斗,使漏斗下端口紧贴烧杯内壁,沿玻璃棒把上述悬浊液慢慢导入漏斗中;该过程中用到的玻璃仪器主要有烧杯、玻璃棒和漏斗等;②蒸发结晶:将上述滤液倒入蒸发皿中,用酒精灯加热蒸发,待蒸发皿中出现较多量晶体时即停止加热;(2)①碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,化学方程式为:Na2CO3+BaCl2=BaCO3↓+2NaCl;②通过分析可知,加入的碳酸钠、氢氧化钠都是过量的,还有生成的氯化钠,所以通过操作Ⅲ所得滤液中的溶质有NaOH、NaCl、Na2CO3;(3)20℃时氯化钠的溶解度为36g,可以通过加入氯化钠固体的方法是溶液达到饱和状态,设需要加入氯化钠为x,![]() =
= ![]() ,解得:x=22.4kg。
,解得:x=22.4kg。
故答案为:(1)漏斗;蒸发皿中出现较多固体(2)Na2CO3+BaCl2=BaCO3↓+2NaCl;NaOH、NaCl、Na2CO3(3)加入22.4 kg的氯化钠固体
(1)根据粗盐提纯的步骤和仪器以及实验的注意事项解答
(2)根据碳酸钠可以除去反应中过量的氯化钡和氯化钙,碳酸钠和氯化钡反应生成碳酸钡和氯化钠解答;根据题中加入的各种除杂试剂进行分析
(3)根据20°是氯化钠的溶解度为36克,计算出所需要的氯化钠


 小学教材全测系列答案
小学教材全测系列答案 小学数学口算题卡脱口而出系列答案
小学数学口算题卡脱口而出系列答案 优秀生应用题卡口算天天练系列答案
优秀生应用题卡口算天天练系列答案 浙江之星课时优化作业系列答案
浙江之星课时优化作业系列答案科目:初中化学 来源: 题型:
【题目】请根据下图实验内容回答下列问题。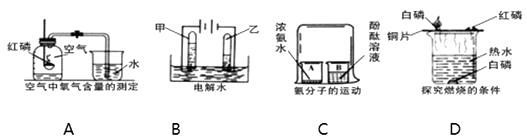
(1)A实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是(填一条即可),该实验不能用蜡烛代替红磷,理由是。
(2)B实验正极产生的气体与负极产生的气体的体积比约为。
(3)C实验观察到的现象是。
(4)D实验资料信息:白磷和红磷的着火点分别是40℃、240℃。铜片上的红磷不燃烧,是因为。水中的白磷不燃烧,是因为。如果要让水中的白磷在水下燃烧,应采取的措施是。通过以上实验事实证明,燃烧一般需要同时具备下列条件:①物质具有可燃性;②可燃物与氧气接触;③。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】矿泉水瓶上一般标有主要矿物成分(单位:mg/L),如 Ca 20、K 39、Mg 3、Zn 0.06、 Fe 0.02 等。这里的 Ca、K、Mg、Zn、Fe 是指 。
A.单质B.元素
C.金属离子D.分子
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】铁的下列性质属于化学性质的是( )
A.具有导电性,能导电B.具有延展性,能拉成丝,也能压成片
C.具有导热性,能制成铁锅D.在潮湿的空气中易生锈
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】工业上可以用食盐和石灰石为原料制取纯碱(Na2CO3),生产的关键是在沉淀池中让NaCl、NH3、CO2和H2O尽可能多地转化成NaHCO3(固体沉淀物)和NH4Cl(溶液),主要生产流程如图所示: 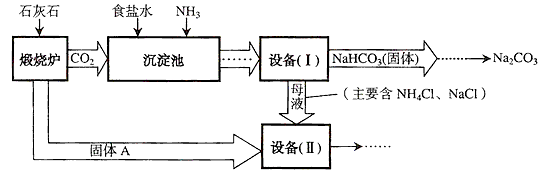
(已知2NH4Cl+Ca(OH)2 ![]() CaCl2+2NH3↑+2H2O)
CaCl2+2NH3↑+2H2O)
(1)“煅烧炉”中发生反应的化学方程式是。
(2)若在实验室里分离“设备(I)”中的混合物,用到的操作名称是。
(3)“沉淀池”中的反应是在加压的条件下不断向食盐水和饱和氨水溶液中通入二氧化碳气体,试分析该流程需要加压条件的原因是。
(4)“设备(Ⅱ)”中固体A与水反应的化学方程式是。
(5)对“设备(Ⅱ)”中的母液处理后,除水以外可在本流程中再利用的物质有(填写化学式)。
(6)请写出一个该生产流程的优点:。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】木炭粉还原氧化铜实验后的混合粉末中含有铜、氧化铜、少量木炭粉,实验室从该混合粉末中回收铜的方案如下:
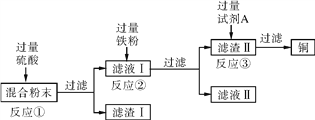
(1)写出下列反应的化学方程式:
反应①:____________________________________________;
反应②:____________________________________________。
(2)反应①所用的硫酸的质量分数为24.5%。现要配制40 g 24.5%的硫酸,需______g 98%的硫酸和______g水。实际操作时,用10 mL量筒取98%的硫酸(密度为1.84 g/cm3),请在图中表示出所取硫酸的体积_____。
![]()
(3)在进行“反应①”“反应②”“反应③” 的操作时,可将反应物加入________(填仪器名称)中,然后______________________(填操作),使反应充分进行。
(4)试剂A可选用__________(填化学式)溶液。
(5)为了从混合粉末中回收更多的铜,可对实验方案进行修改和完善,你的建议是(提出一条即可)______________________________________________________。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列关于催化剂的说法正确的是()
A.催化剂不能改变生成物的质量B.催化剂只能加快化学反应速率,但本身的性质不变
C.二氧化锰可作任何反应的催化剂 D.没有催化剂就不能进行化学反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com