
分析 根据图示测得的相关数据及相关的过氧化氢分解的化学方程式,依据质量守恒定律计算生成氧气的质量,再根据已知的氧气质量代入化学方程式求得参加反应的过氧化氢的质量,最后可求得过氧化氢溶液中溶质的质量分数.
解答 解:(1)由于二氧化锰是反应的催化剂,质量不变,所以,剩余的混合物中二氧化锰的质量为1.0g,根据质量守恒定律,减少的质量就是生成的氧气的质量即:68.0g+1.0g-67.4g=1.6g
(2)该化学反应方程式为:2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)设68.0 g过氧化氢溶液中含有过氧化氢的质量为x.
2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑
68 32
x 1.6g
$\frac{68}{x}=\frac{32}{1.6g}$
解得:x=3.4g
过氧化氢溶液的溶质的质量分数=$\frac{3.4g}{68g}$×100%═5%.
答案:
(1)1.0g,1.6;
(2)2H2O2 $\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)5%.
点评 解此题的关键是根据图示测得的相关数据及质量守恒定律计算出隐藏的已知量---生成的氧气质量;进而按化学方程式的解题格式解答即可.


 全能练考卷系列答案
全能练考卷系列答案 一课一练课时达标系列答案
一课一练课时达标系列答案科目:初中化学 来源: 题型:解答题
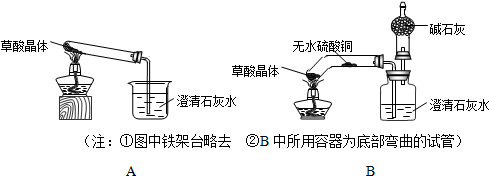
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
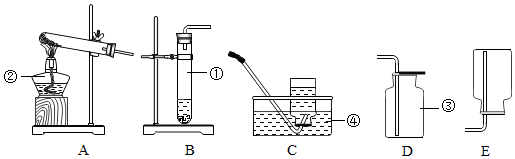
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
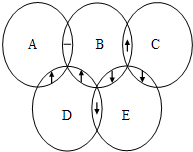 如图中A、B、C、D、E分别是Na2CO3、(NH4)2CO3、BaCl2、H2SO4、NaOH五种溶液中的一种,两圆的相交部分为两种溶液反应出现的主要实验现象(“↓”表示有沉淀生成、“↑”表示有气体生成、“-”表示无明显现象).
如图中A、B、C、D、E分别是Na2CO3、(NH4)2CO3、BaCl2、H2SO4、NaOH五种溶液中的一种,两圆的相交部分为两种溶液反应出现的主要实验现象(“↓”表示有沉淀生成、“↑”表示有气体生成、“-”表示无明显现象).查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 操作步骤 | 实验现象 | 结论 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com