
| 时间/s | 0 | 20 | 30 | 40 | 60 | 80 | 100 | 120 |
| 增加的质量/g | 0 | 0.7 | m | 1.2 | 1.5 | 1.6 | 1.7 | 1.7 |
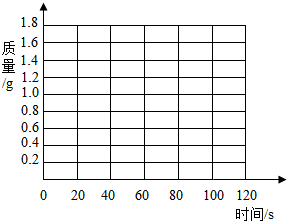
分析 (1)利用数据表中测得的时间与增加的质量,找出对应的点并用平滑曲线连接;
(2)利用所绘制的曲线,查出时间为30s时所增加的质量;
(3)根据反应的化学方程式,由生成氨气的质量计算出样品中硝酸铵的质量,利用硝酸铵样品的纯度=$\frac{硝酸铵的质量}{样品质量10g}$×100%计算样品纯度;
(4)根据反应的化学方程式,由生成氨气的质量计算反应生成硝酸钠的质量,利用所得硝酸钠溶液的溶质质量分数=$\frac{硝酸钠的质量}{反应所得溶液质量}$×100%,反应后所得溶液质量可利用质量守恒定律进行计算而求得.
解答 解:(1)根据测定数据表中的时间与质量数据确定一些点,然后把各点利用平滑曲线图连接;绘制曲线时要做到:曲线平滑、趋势正确、给出平台;
故答案为: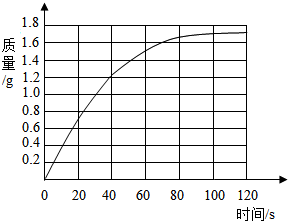
(2)根据所绘制的曲线,可估计反应进行至30s时,增加的质量约为1.0g;
故答案为:1.0g;
(3)放出1.7gNH3消耗硝酸铵的质量为m,所得硝酸钠的质量为x
NH4NO3+NaOH$\frac{\underline{\;\;△\;\;}}{\;}$NaNO3+H2O+NH3↑
80 85 17
m x 1.7g
$\frac{80}{m}=\frac{17}{1.7g}$
m=8g
硝酸铵样品的纯度=$\frac{8g}{10g}$×100%=80%
故答案为:80%;
(4)$\frac{85}{x}=\frac{17}{1.7g}$
x=8.5g
反应后所得硝酸钠溶液的溶质质量分数=$\frac{8.5g}{10g×80%+30g+13.7g-1.7g}$×100%=17%
答:反应后所得硝酸钠溶液的溶质质量分数为17%.
点评 根据质量守恒定律,反应后所得硝酸钠溶液的质量=样品中硝酸铵的质量+溶解所加水的质量+氢氧化钠浓溶液的质量-反应放出氨气的质量.


科目:初中化学 来源: 题型:选择题
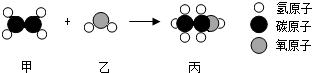
| A. | 该反应属于化合反应 | |
| B. | 该反应中分子和原子的种类都发生了改变 | |
| C. | 甲中碳、氢两元素的质量比为6:1 | |
| D. | 甲、丙分别在氧气中完全燃烧,产物相同 |
查看答案和解析>>
科目:初中化学 来源: 题型:推断题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A | B | C | D |
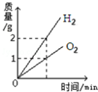 |  | 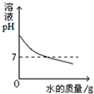 | 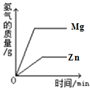 |
| 电解水生成氢气和氧气的质量与反应时间的关系 | 加热一定质量高锰酸钾固体制氧气,剩余固体中锰元素的质量分数与反应时间的关系 | 向氢氧化钠溶液中不断加水,溶液pH与加入水的质量关系 | 相同质量的Mg、Zn分别与足量的稀盐酸反应,产生氢气的质量与反应时间的关系 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cu+2AgCl═CuCl2+2Ag | B. | BaCl2+2KOH═Ba(OH)2+2KCl | ||
| C. | 4Fe+3O2$\frac{\underline{\;点燃\;}}{\;}$2Fe2O3 | D. | 2NaOH+SO2═Na2SO3+H2O |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com