
分析 根据活动性强的金属可以把活动性弱的金属从其盐溶液中置换出来,所以锌可以置换出银,但不能置换出铝,充分反应后过滤,向滤出的固体中滴加稀盐酸,有气泡产生,此现象说明锌过量,所以原混合溶液中的AgNO3全部被置换生成Ag和Zn(NO3)2溶液,A1(NO3)3不反应进行分析.
解答 解:锌可以置换出银,但不能置换出铝,充分反应后过滤,向滤出的固体中滴加稀盐酸,有气泡产生,此现象说明锌过量,所以原混合溶液中的AgNO3全部被置换生成Ag和Zn(NO3)2溶液,A1(NO3)3不反应,所以滤液中含有的金属离子有Al3+ 和Zn2+;化学方程式为:Zn+2AgNO3=Zn(NO3)2+2Ag(或Zn+2HCl=ZnCl2+H2↑).
故答案为:Al3+ 和Zn2+;
Zn+2AgNO3=Zn(NO3)2+2Ag(或Zn+2HCl=ZnCl2+H2↑).
点评 本题是对金属活动性顺序的考查,解题的关键是掌握金属活动性顺序表的意义,只有这样才能做出正确的判断.


科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 ”)表示相连物质间可以反应,“→”表示物质间可以转化(注:反应条件、部分反应物或生成物略去).
”)表示相连物质间可以反应,“→”表示物质间可以转化(注:反应条件、部分反应物或生成物略去).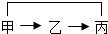 ,甲、乙、丙为不同类别的化合物,甲→乙、乙→丙均为复分解反应,则甲与丙反应的化学方程式为Ca(OH)2 +CO2═CaCO3↓+H2O.
,甲、乙、丙为不同类别的化合物,甲→乙、乙→丙均为复分解反应,则甲与丙反应的化学方程式为Ca(OH)2 +CO2═CaCO3↓+H2O.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| (1)称取上述固体样品8g溶于100mL水配成溶液,向溶液中滴加过量的氯化钙溶液充分反应后,静置. | 产生白色沉淀① | 说明久置固体中,一定含有Na2CO3 |
| (2)用玻璃棒蘸取少量①中的上层清液滴在pH试纸上,与标准比色卡对比,测出pH | pH=10 | 说明固体中,还一定含有 ②NaOH(填化学式). |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 汞使用的历史悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )
汞使用的历史悠久,用途很广泛,在元素周期表中,汞元素的信息如图所示,对图中信息解释正确的是( )| A. | 汞元素非金属元素 | B. | 汞原子的核外电子数是80 | ||
| C. | 汞原子核内中子数是80 | D. | 汞原子的相对原子质量是200.6g |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| 1将NaOH溶液稀释,滴人该酚酞溶液. | 溶液变红,继续滴加酚酞溶液,红色消失 | 甲同学猜想不正确 (填“正确”或“不正确”) |
| 2向澄清石灰水中滴入该酚酞溶液 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com