
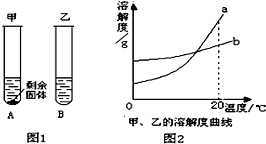
 20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.
20℃时,分别向盛有10g水的两支试管中,加入等质量的甲、乙两种固体物质,使其充分溶解,可观察到如图所示的现象.| 实验序号 | 水的质量(g) | 加入NaCl的质量(g) | 溶液的质量(g) |
| ① | 10 | 2 | 12 |
| ② | 10 | 3 | 13 |
| ③ | 10 | 4 | 13.6 |
| ④ | 10 | 5 | 13.6 |
分析 溶液中有未溶解的固体溶质的溶液为不能再溶解该溶质的饱和溶液;交点的含义是两物质的溶解度在该温度下相等;根据20℃甲、乙物质的溶解现象判断两物质的溶解度曲线,根据曲线表现出来的溶解度与温度变化关系,选择把甲物质继续溶解的方法.
由表中数据可知,随着氯化钠的不断加入,溶液的质量在增加,当10g水中溶解了3.6g氯化钠后不再溶解,说明已经达到饱和状态
解答 解:(1)充分溶解后,甲物质有剩余,没有全部被溶解,说明此时甲的溶液为饱和溶液;
(2)20℃10g水溶解较多的乙物质,说明此时物质乙的溶解度比物质甲大,则a曲线表示的是乙,b曲线表示的是甲,由于甲的溶解度随着温度的升高而增大,故可通过升温或增加水的方法把未溶解的甲物质溶解.
(3)A、由③中数据可知,②中所得溶液是不饱和溶液,故选项错误;
B、20℃时10g水最多能溶解3.6gNaCl,故选项错误;
C、由表中数据可知,③④溶液都是饱和溶液,在相同温度下,同种物质的饱和溶液的溶质质量分数相等,故选项正确;
D、①所得溶液的溶质质量分数为:$\frac{2g}{12g}×$100%=16.7%,故选项错误.
故选C
故答案为:
(1)A;
(2)b;增加水;
(3)C.
点评 固体物质加入水中充分溶解后,溶液中仍有未溶解的固体溶质的溶液一定为该温度下的饱和溶液.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:初中化学 来源: 题型:选择题
| A. | 导电的物质都是金属 | B. | 有一定熔点的固体都是晶体 | ||
| C. | 橡胶、塑料都是合成材料 | D. | 含氧元素的化合物都是氧化物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 不饱和溶液转化为饱和溶液,其溶质的质量分数一定增大 | |
| B. | 饱和溶液析出晶体后,溶质的质量分数一定减小 | |
| C. | 只要温度不变,某饱和溶液中固体溶质的溶解度一定不变 | |
| D. | 降温时,饱和溶液一定会析出晶体 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
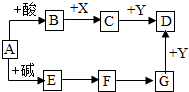 如图是初中化学常见物质间的转化关系(反应条件和部分产物已略),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态,请回答下列问题:
如图是初中化学常见物质间的转化关系(反应条件和部分产物已略),其中A为钠盐,X、Y均为黑色粉末,D为红色金属单质,F在常温下为液态,请回答下列问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A.生活中的物质 | B.安全常识 | C.元素与人体健康 | D.日常生活经验 |
| 铅笔芯主要成分--石墨 饮水机滤芯的吸附剂主要成分--活性炭 | 进入陌生溶洞前--先做灯火实验 闻试剂气味--鼻子尽量靠近试剂瓶口 | 缺铁--易引起贫血 缺碘--易患甲状腺肿大 | 区别老陈醋与酱油--闻气味 区分羊毛纤维与合成纤维-灼烧后闻气味 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 镁带在空气中燃烧发出耀眼白光 | |
| B. | 红磷在空气中燃烧产生大量白烟 | |
| C. | 稀硫酸滴入石蕊试液后溶液变蓝 | |
| D. | 打开浓盐酸的瓶盖瓶口出现大量白雾 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
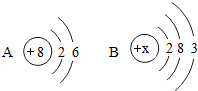 如图为A、B两种元素的原子结构示意图,请据图回答下列问题:
如图为A、B两种元素的原子结构示意图,请据图回答下列问题:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com