
【题目】聚合硫酸铁(PFS)是一种新型的饮用水处理剂和城市污水净化剂,其化学组成可表示为[Fex(OH)y(SO4)z]m。某中学化学兴趣小组以聚合硫酸铁的生产流程和相关性质进行了一系列的探究。
Ⅰ.聚合硫酸铁的工业生产。
如图是以回收废铁屑为原料制备PFS的一种工艺流程。
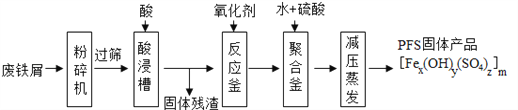
回答下列问题
(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为______。“过筛”与化学实验中的______原理相似(填操作名称)。
(2)酸浸时最合适的酸是______,写出铁锈与该酸反应的化学反应方程式______。
(3)反应釜中加入氧化剂的作用是将Fe2+转化为Fe3+。你认为下列氧化剂中最合适的是
______(填标号),原因是______。
A.KMnO4 B.Cl2 C.H2O2 D.HNO3
(4)相对于常压蒸发,减压蒸发的优点是______。
A.有利于水分蒸发 B.降低沸点,防止晶体分解 C.降低生产成本
Ⅱ.聚合硫酸铁的成分探究。
该研究小组为确定聚合硫酸铁的化学式,进行了如下实验:
①称取5.52 g聚合硫酸铁样品溶于足量的稀盐酸中并充分混合;
②向①所得的混合物中加入足量的BaCl2溶液,充分反应后,经过滤、洗涤、干燥、称重,得沉淀4.66 g。
③若向步骤②的滤液中加入过量的NaOH溶液,充分反应后,再将沉淀过滤、洗涤、灼烧、称重,得固体3.20 g。
则聚合硫酸铁[Fex(OH)y(SO4)z]m样品中的x:y:z的值为______。
试写出该聚合硫酸铁与盐酸的反应方程式______。
Ⅲ.聚合硫酸铁的热分解气体产物成分探究。
该小组将5.52 g聚合硫酸铁在一定条件下加热完全分解,对所得气体产物进行实验探究。(已知SO3的熔点为16.8℃)。
【提出假设】
假设1:所得气体的成分是SO3;
假设2:所得气体的成分是SO2、O2;
假设3:所得气体的成分是______。
【设计实验】
按下图装置进行实验。
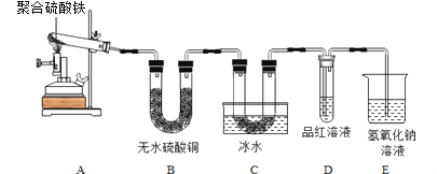
实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是______。
【实验结论】
通过实验现象判断,假设______成立。
如果最终试管中固体为一种红棕色纯净物,则质量为______。
【答案】 三氧化二铁 过滤 稀硫酸 Fe2O3 + 3H2SO4 = Fe2(SO4)3 + 3H2O C 不引入其他杂质 AB 2:4:1 3[Fe2(OH)4SO4]m + 12m HCl = m Fe2(SO4)3 + 4m FeCl3 + 12m H2O SO3、SO2、O2 吸收多余的二氧化硫,防止污染空气 3 3.2 g
【解析】根据所学知识和题中信息知,Ⅰ.聚合硫酸铁的工业生产。(1)废铁屑主要为表面附有大量铁锈的铁,铁锈的主要成分为三氧化二铁。“过筛”与化学实验中的过滤原理相似。(2)酸浸时最合适的酸是稀硫酸,铁锈与该酸反应的化学反应方程式是Fe2O3 + 3H2SO4 = Fe2(SO4)3 +3H2O 。(3)反应釜中加入氧化剂的作用是将Fe2+转化为Fe3+。下列氧化剂中最合适的是C.H2O2 ,原因是不引入其他杂质。(4)相对于常压蒸发,减压蒸发的优点是A.有利于水分蒸发。 B.降低沸点,防止晶体分解。Ⅱ.聚合硫酸铁的成分探究。聚合硫酸铁[Fex(OH)y(SO4)z]m样品中的x:y:z的值为∶根据化合物中正负化合价代数和为零原则,3x=y+2z, x:y:z的值为2:4:1 。该聚合硫酸铁与盐酸的反应方程式是. 3[Fe2(OH)4SO4]m + 12m HCl = m Fe2(SO4)3 + 4m FeCl3 + 12m H2O 。Ⅲ.聚合硫酸铁的热分解气体产物成分探究。【提出假设】假设1:所得气体的成分是SO3;假设2:所得气体的成分是SO2、O2;假设3:所得气体的成分是SO3、SO2、O2。实验过程中发现:B中无水硫酸铜变蓝,C中U形管内有无色晶体析出,D中品红溶液褪色,装置E的作用是吸收多余的二氧化硫,防止污染空气。【实验结论】通过实验现象判断,假设3成立。如果最终试管中固体为一种红棕色纯净物,则质量为3.2 g。
点睛∶本题主要考查聚合硫酸铁的工业生产,聚合硫酸铁的成分探究,聚合硫酸铁的热分解气体产物成分探究。


科目:初中化学 来源: 题型:
【题目】甲烷是最简单的有机物,实验室常用加热无水醋酸钠和碱石灰的固体混合物制取甲烷。在标准状况下,甲烷的密度比空气密度小,难溶于水。某实验小组准备了下列器材进行甲烷的制取和收集实验。

(1)在图A所示的装置中,仪器①的名称是___________。
(2)实验室中制取并收集比较纯净的甲烷可选用下列仪器中的_______和______。(填编号)
(3)请你设计实验,检验生成的气体甲烷中含有氢元素。
实验操作 | 实验现象 | 实验结论 |
______ | _____ | 甲烷中含有氢元素 |
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】煤、石油和天然气是重要的、不可再生的能源,它们燃烧产生过多的二氧化碳等物质会对环境造成严重的影响。我国政府高度重视“节能减排”,确定我国今年“世界环境日”的主题和标识。
(1)下列措施符合我国“世界环境日”主题的是____________。(填字母)
A.限制发展高耗能的产业
B.推广使用“乙醇汽油”,减少有害气体排放
C.为了减少废气对本地区空气的污染, 化工厂加高烟囱
D.将污染严重的工厂迁到农村去
(2)天然气的主要成分是_______(填名称),其完全燃烧的化学方程式为_____________。
(3)图2中的信息告诫人类:二氧化碳等气体过多的排放,使_______________加剧,导致全球变暖。为减少二氧化碳过多的排放对环境的影响,你能做的一件事____________________;科学家采取“组分转化”技术,将二氧化碳和氢气以一定比例混和,在一定条件下反应,生成一种重要的化工原料乙烯(C2H4)和水。该反应的化学方程式为_____________________________。
(4)为解决能源短缺和环境污染的问题,目前有待开发、利用的新能源有_______________。(写一种)
(5)“绿箱子环保计划——废弃手机及配件回收联合行动”已在全国许多重点城市中相继开展,废弃手机中的金属材料回收利用的意义,你认为有_______________(举出一个方面)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】甲图是一氧化碳还原氧化铁的装置,乙图是炼铁高炉示意图。下列叙述中正确的是
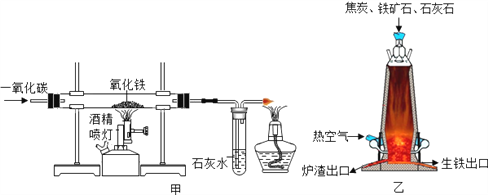
A. 炼铁的主要原理是:3CO+Fe2O3高温2Fe+3CO2
B. 乙图炼铁中原料焦炭的作用是只提供热量
C. 甲图中实验开始时应先点燃加热氧化铁的酒精喷灯
D. 两图中得到的铁是完全相同的
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】请沿用科学家认识事物的方式认识“空气”。
(1)从空气组成角度:某同学利用红磷测定空气中氧气的含量,实验装置如图所示。

①实验原理:______(用化学方程式表示)。
②实验步骤:先用弹簧夹夹住橡皮管,点燃红磷,伸入瓶中并塞上瓶塞。等红磷燃烧熄灭后再打开弹簧夹。
③误差分析:发现实验结论大于理论值,可能的原因有______。
A.装置漏气
B.实验时使用的红磷过量
C.实验时插入燃烧匙的速度太慢,集气瓶内部分空气受热逸出
D.红磷熄灭后没等集气瓶冷却就立刻打开弹簧夹
(2)从微观角度:用“![]() ”表示氮原子,“
”表示氮原子,“![]() ”表示氧原子。
”表示氧原子。
① 用“![]() ”可表示的微粒是______(填名称)。
”可表示的微粒是______(填名称)。
② 同温同压下,气体的体积比等于分子数目比。若空气中其它成分忽略不计,下图可表示空气微观模型的是______(填标号)。

(3)从变化角度:
已知:常压下,氮气沸点-196℃,氧气沸点-183℃。将燃着的木条置于盛满液态空气的烧杯口,观察到的现象是______。将该烧杯放置一段时间后,液态物质剩余约1/10体积,其主要成分是______。
(4)从应用角度:利用空气制取氮肥的流程下图所示。

① Ⅰ中参加反应的单质甲为______。
② Ⅱ中反应的化学方程式为______。
③ 物质所含元素化合价发生变化的反应称为氧化还原反应。反应Ⅲ______(填“属于”或“不属于”)氧化还原反应。
(5)从环保角度:下列保护空气措施合理的是______(填标号)。
A.工厂通过加高烟囱直接排放废气
B.推广使用乙醇汽油代替普通汽油
C.提倡步行、骑自行车等“低碳”出行方式
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】形成化学观念是化学学习的任务之一,下列说法错误的是
A. 金刚石和石墨组成元素相同,性质也完全相同
B. 分子、原子、离子都是构成物质的微粒
C. 化学变化的过程实质上是原子重新组合的过程
D. 等体积的酒精和水混合后体积小于混合前二者体积之和,是因为分子间存在间隔
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下列广告词对应商品的主要成分及类别不正确的是
选项 | 广告词 | 商品 | 主要成分 | 类别 |
A. | “衡水老白干,喝出男人味” | 白酒 | 乙醇 | 有机物 |
B. | “特别的味,给特别的您” | 凤利酥 | 淀粉 | 蛋白质 |
C. | “补钙新一代,骨康都期待” | 补钙剂 | 碳酸钙 | 盐 |
D. | “农夫山泉有点甜” | 矿泉水 | 水 | 化合物 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com