取一定质量的CO和CO2的混合气体,通入足量的Ba(OH)2溶液中,充分反应后过滤,发现生成的沉淀和所取的混合气体质量相等.求混合气体中,碳原子与氧原子的个数比.
分析:CO和CO2的混合气体,通人足量的Ba(OH)2溶液中,充分反应后过滤,所得沉淀为二氧化碳与氢氧化钡反应生成碳酸钡;生成的沉淀和所取的混合气体质量相等,即生成碳酸钡的质量与混合气体的质量相等.通过假设碳酸钡的质量,根据反应化学方程式,求得混合气体中所取CO和CO2的混合气体中质量关系,从而利用两气体中C、O元素质量比得出混合气体中C、O元素质量关系,最后利用C、O元素的相对原子质量求出混合气体中碳原子与氧原子的个数比.
解答:解:假设充分反应后生成碳酸钙的质量为m,设混合气体中二氧化碳质量为x
CO
2+Ba(OH)
2═BaCO
3↓+H
2O
44 197
x m
=
x=
则混合气体中CO的质量=m-
=
则混合气体中C、O元素质量比=
| ××100%+ ××100% |
| ××100%+××100% |
=543:836
则混合气体中C、O原子个数比=
:
=181:209
答:混合气体中,碳原子与氧原子的个数比为181:209.
点评:由于题中生成的沉淀和所取的混合气体质量相等,该问题的焦点集中到混合气体的质量与反应生成的碳酸钡的质量上,如果有了碳酸钡的质量,一切问题都会迎刃而解.



 探究与巩固河南科学技术出版社系列答案
探究与巩固河南科学技术出版社系列答案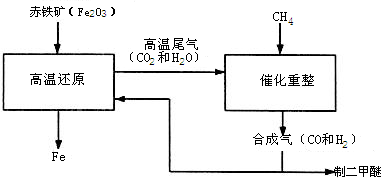
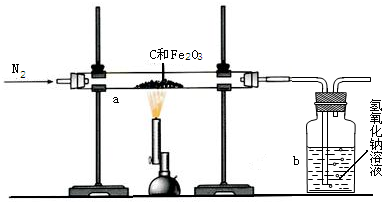
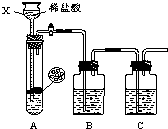 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.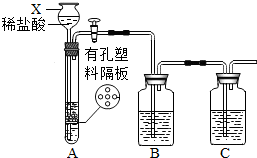 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.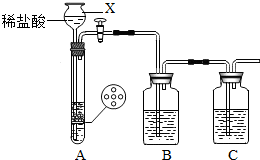 (2012?崇川区一模)某研究性学习小组设计并进行了如下实验.
(2012?崇川区一模)某研究性学习小组设计并进行了如下实验.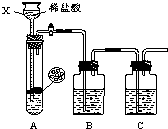 某研究性学习小组设计并进行了如下实验.
某研究性学习小组设计并进行了如下实验.