
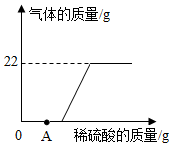
 实验后的废液一般需回收处理,不能直接倒入排污管.小明实验后收集到含有碳酸钾和氧氧化钾的废水样品50g,他向废液中缓缓滴入溶质质量分数为10%的稀硫酸,生成二氧化碳质量与滴入稀硫酸质量的关系如图所示,当废液恰好处理完毕时,溶液总质量为194.8g,溶于水的气体忽略不计,则:
实验后的废液一般需回收处理,不能直接倒入排污管.小明实验后收集到含有碳酸钾和氧氧化钾的废水样品50g,他向废液中缓缓滴入溶质质量分数为10%的稀硫酸,生成二氧化碳质量与滴入稀硫酸质量的关系如图所示,当废液恰好处理完毕时,溶液总质量为194.8g,溶于水的气体忽略不计,则:分析 (1)碳酸钾和氢氧化钾都能与稀硫酸反应,氢氧化钾优先与硫酸反应;
(2)根据气体的质量结合化学方程式计算碳酸钾的质量和与碳酸钾反应的硫酸的质量;
(3)依据氢氧化钾反应的硫酸的质量与化学方程式可以计算氢氧化钾的质量.
解答 解:(1)碳酸钾和氢氧化钾都能与稀硫酸反应,氢氧化钾优先与硫酸反应,图中A处为硫酸不足,氢氧化钾有剩余,所以图中A处溶液中溶质的成分K2SO4、K2CO3、KOH;故选:K2SO4、K2CO3、KOH;
(2)由图可知生成二氧化碳的质量为2.2g,
设废水样品中碳酸钾的质量为x;与碳酸钾反应的硫酸的质量为y
K2CO3+H2SO4=K2SO4+H2O+CO2↑
138 98 44
x y 2.2g
$\frac{138}{x}=\frac{98}{y}=\frac{44}{2.2g}$
x=6.9g,y=4.9g
(3)恰好反应时稀硫酸的质量为194.8g+2.2g-50g=147g
与氢氧化钾反应的硫酸的质量为147g×10%-4.9g=9.8g,
设废水样品中氢氧化钾的质量为z
H2SO4+2KOH═K2SO4+2H2O
98 112
9.8g z
$\frac{98}{9.8g}=\frac{112}{z}$
z=11.2g
答:废水样品中碳酸钾的质量为6.9g;废水样品中氢氧化钾的质量为11.2g.
点评 在解此类题时,首先分析反应应用的原理,然后结合图象中的转折点,以及方程式中的比例关系进行解答.


 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2CO3→NaCl→NaNO3→NaOH | B. | C→CO→Fe→Fe2O3 | ||
| C. | Cu→CuO→CuSO4→Cu(OH)2 | D. | CaCO3→CaO→Ca(OH)2→NaOH |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
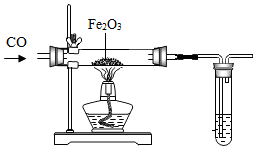 冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.
冶炼金属通常是指从矿石中提取金属单质的过程,除“沙土淘金”等物理方法外,金属冶炼大都是使金属从其化合态(化合物)转化为游离态(单质)的化学过程.根据金属的化学性质不同,工业上冶炼金属一般有以下几种方法.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 锌可以与稀盐酸反应生成氢气,所以锌也可以与稀硫酸反应生成氢气 | |
| B. | 中和反应生成盐和水,故生成盐和水的反应一定是中和反应 | |
| C. | 碱溶液能使无色酚酞溶液变红,则能使无色酚酞溶液变红的溶液一定是碱溶液 | |
| D. | 硫酸可以与BaCl2反应生成沉淀,所以盐酸也可以与BaCl2反应生成沉淀 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CuSO4 KNO3 HCl Na2SO4 | B. | NaOH NaCl HCl FeCl3 | ||
| C. | NaNO3 HCl Na2SO4 H2SO4 | D. | K2CO3 H2SO4 CaCl2 Na2CO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com