
【题目】2018年2月9日,歼﹣20开始列装空军作战部队。它是一款具备高隐身性、高态势感知、高机动性的隐形第五代战斗机。其隐身材料是目前最新的纳米高分子复合材料。芳纶是一种可做此材料的新型高科技特种纤维,可由间苯二甲酰氯和间苯二胺缩聚而成。其中,间苯二胺的化学式是C6H8N2,试回答:

①间苯二胺属于_____(填写“单质”“氧化物”“有机物”)之一。
②间苯二胺由_____种元素组成。
③间苯二胺分子中,N、H两种原子的个数之比为_____(填最简整数比)。
④间苯二胺中,碳元素和氢元素的质量之比为_____(填最简整数比)。
⑤间苯二胺中,所含元素质量分数最大的元素是_____。
【答案】有机物 三 1:4 9:1 碳或C
【解析】
①由间苯二胺的化学式可知,它是一种由碳、氢、氮三种元素组成的化合物,是含碳元素的化合物,属于有机物;故填:有机物;
②间苯二胺的化学式是C6H8N2,由C、H、O三种元素组成。故填:三;
③根据间苯二胺的化学式C6H8N2可以看出,每个间苯二胺分子中氮、氢两种原子个数比为2:8=1:4,故填:1:4;
④由间苯二胺的化学式可知,间苯二胺是由碳、氢、氮三种元素组成的,其中碳、氢两元素的质量比为(12×6):(1×8)=9:1;故填:9:1;
⑤间苯二胺中碳、氢、氮三元素的质量比是(12×6):(1×8):(14×2)=9:1:3,可知其中碳元素的质量分数最大;故填:碳或C。


科目:初中化学 来源: 题型:
【题目】小川同学用实验探究铁、镁、铜三种金属的活动性顺序时,将有关反应记录如下:
Fe+2HCl=FeCl2+H2↑ Mg+2HCl=MgCl2+H2↑ Fe+CuSO4= FeSO4+Cu Cu+2HCl![]() 不反应
不反应
(1)从上述反应中,可获得的信息有(至少两条)____________;
(2)通过观察实验现象,能说明镁比铁活泼的依据是____________;如果补充一个实验(用化学方程式)___________,也能说明镁比铁活泼。
(3)用金属活动顺序解释生活中的一些现象,如:_____________
(4)使用铁锅有利于人体健康,主要原因是______________
(5)人们大量使用的是合金,这是因为合金具有更多优良性能,如钢比纯铁的硬度_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】已知碳酸氢钠受热易分解,而碳酸钠热稳定性好.取碳酸氢钠和碳酸钠的混合物10.0g,加热到固体质量不再改变为止,得剩余固体6.9g.下列说法正确的是( )
A. 剩余固体为混合物
B. 反应后生成CO2的质量为3.1g
C. 原混合物中NaHCO3和Na2CO3质量比为21:29
D. 反应前后的固体分别与相同浓度稀盐酸恰好完全反应所需盐酸质量相同
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为A物质的溶解度曲线。M、N两点分别表示A物质的两种溶液。下列做法能实现M、N之间相互转化的是( )
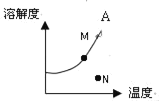
A. 从N→M:先向N 中加入适量固体A,再升温
B. 从N→M:先将N升温,再加入适量固体A
C. 从M→N:先将M降温后过滤,再将其升温
D. 从M→N:先将M 升温,再将其蒸发部分水
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是A、B、C三种固体物质的溶解度曲线:请回答下列问题:
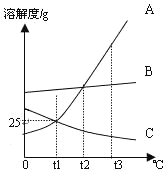
(1)t1℃时A物质的饱和溶液中溶液质量与溶剂质量的比(最简比)_____。
(2)B物质中混有少量A物质时,可采用_____ 方法得到较纯净的B物质。
(3)t1℃时A、B、C三种物质的饱和溶液同时升温到t2℃此时溶液中溶质的质量分数大小关系是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学就在我们身边,人类的衣、食、住、行都离不开化学。
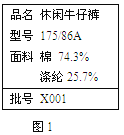
(1)某服装标签如图1,该服装面料含有的合成纤维是_____(填“棉“或“涤纶“):新衣服拿在手里,有时能闻到特殊气味,能闻到气味的原因是_____。
(2)在宏观、微观和符号之间建立联系是学习化学的基本方法。下列为A、B、C、D的原子或离子的结构示意图。

①B的原子结构示意图中X为_____; D图表示的微粒符号是_____。
②分析A、B、C、D的原子或离子的结构示意图,你认为具有相似化学性质的微粒是_____ (填字母序号)。
(3)“西气东输”后,家庭用上了天然气,灶具开关通过电子打火引燃天然气,此过程满足燃烧的条件是:_____;天然气燃烧反应的化学方程式为_____。
(4)从海水中提取粗盐一般可采用_____方法,其中含量最多的阴离子符号是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图为某反应的微观模拟示意图。下列从图中获得的有关信息中,不正确的是( )
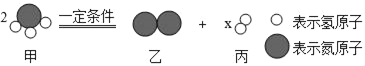
A. 图示中X的数值为3
B. 该化学反应类型属于分解反应
C. 该反应中分子和原子的种类都发生了改变
D. 该反应前后各元素的化合价都发生了变化
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】小华同学配制50g溶质质量分数为20%的NaCl溶液,操作流程如图:

(1)小华同学应称取的NaCl质量为________g。
(2)指出图中的一处错误:________。
(3)用托盘天平称量所需的氯化钠时,发现托盘天平的指针偏向左盘,应________。
A 增加适量氯化钠固体 B 减少适量氯化钠固体 C 调节平衡螺母
(4)在用量筒量取水的过程中,当液面接近刻度线时,他的操作如图所示,其中规范的是____(填序号)。
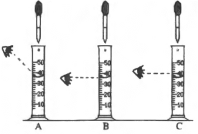
(5)如果小华配制的氯化钠溶液的溶质质量分数小于20%,则造成此误差的可能原因有______(填序号)。
A 配制溶液的烧杯内壁湿润
B 称量纸上残留少量食盐
C 向烧杯中加水时,有少量水溅出烧杯外
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如表是元素周期表的一部分:

(1)很多科学家对元素周期表的发现和完善作出了重大贡献,写出其中一位科学家的名字_____。
(2)12号元素的元素符号为_____;B元素的相对原子质量为_____;相对原子质量为22.99的元素属于_____(填“金属”或“非金属”)元素,其原子在化学反应中容易_____(填“得到”或“失去”)电子;Ne的化学性质_____(填“稳定”或“不稳定”)
(3)利用元素周期表,人们对元素的认识进入全新的飞跃时期,科学家相继合成了很多新的元素。他们合成了第118号元素,该元素的核电荷数为_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com