

分析 (1)根据配制溶液的一般步骤可以完成解答;
(2)氢氧化钠和硫酸铜溶液反应生成了硫酸钠和氢氧化铜承担,可以据此写出该反应的化学方程式,结合硫酸铜的质量计算出氢氧化钠的质量、生成的硫酸钠、氢氧化铜的质量,进而求出氢氧化钠溶液中溶质的质量分数、反应后所得溶液中溶质质量分数.
解答 解:(1)配制硫酸铜溶液时,计算完后,取药品进行称量,称量时先称固体盐,后量取水,最后是溶解,故步骤为:称量、量取、溶解.结合图示正确的操作顺序是e c b a d.
(2)①CuSO4溶液中所含CuSO4质量为:80g×10%=8g
设氢氧化钠溶液中氢氧化钠的质量为x,生成的硫酸钠的质量为y,生成的氢氧化铜的质量为z
CuSO4+2NaOH═Na2SO4+Cu(OH)2↓
160 80 142 98
8g x y z
$\frac{160}{8g}=\frac{80}{x}=\frac{142}{y}=\frac{98}{z}$
解得:x=4g y=7.1g z=4.9g
氢氧化钠溶液中溶质的质量分数:$\frac{4g}{50g}×100%$=8%
②反应后所得溶液中溶质质量分数是:$\frac{7.1g}{50g+80g-4.9g}×100%$≈5.68%
答:NaOH溶液中溶质的质量分数为8%.
答案:(1)e c b a d;(2)①氢氧化钠溶液中溶质的质量分数8%.②反应后所得溶液中溶质质量分数是5.68%.
点评 根据反应的化学方程式可以反映出各物质的质量关系,由反应中某种物质的质量可计算出反应中其它物质的质量.


 名校课堂系列答案
名校课堂系列答案科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 用盐酸除去铁锈 | B. | 用含氧化镁的药物治疗胃酸过多 | ||
| C. | 用碳酸钙作补钙剂 | D. | 用氨水(NH3•H2O)处理工厂的硫酸 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
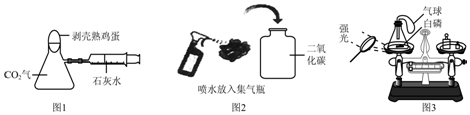
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
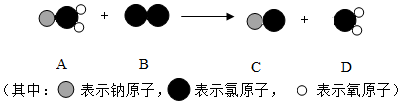
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
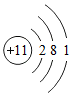 图为某元素的原子结构示意图,下列说法错误的是( )
图为某元素的原子结构示意图,下列说法错误的是( )| A. | 它的阳离子带1个单位正电荷 | B. | 它的阳离子有10个质子 | ||
| C. | 它是一种金属元素 | D. | 它的原子核外有11个电子 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com