
下列氯化钠溶液,其溶质的质量分数不等于15%的是……………………………( )
A.100 g水中溶解15 g氯化钠
B.氯化钠与水按15:85的质量比形成的溶液
C.100 g 溶液中含15 g氯化钠
D.30 g氯化钠溶解于170 g水中所形成的溶液
 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案科目:初中化学 来源: 题型:阅读理解
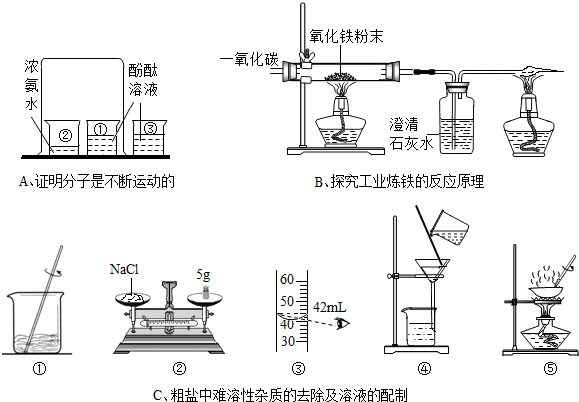
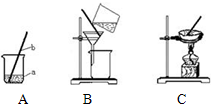 (1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.
(1)在做粗盐初步提纯的实验时,要进行如图所示的实验操作.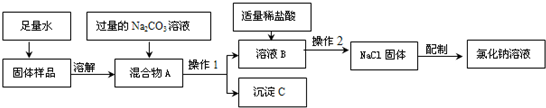
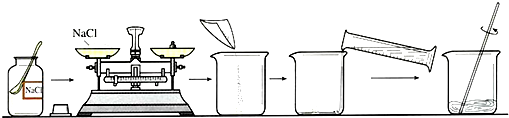
查看答案和解析>>
科目:初中化学 来源: 题型:
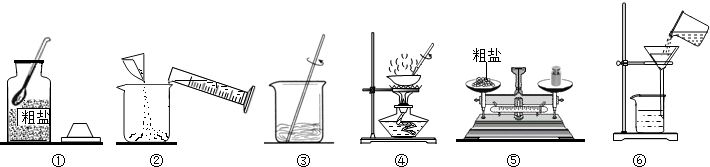
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com