
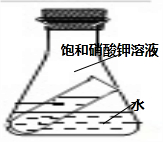
 明明同学设计了如图所示的装置进行趣味实验.
明明同学设计了如图所示的装置进行趣味实验.分析 根据氢氧化钙的溶解度随温度的升高而减小,硝酸钾的溶解度随温度的升高而增大进行分析.
解答 解:(1)硝酸铵溶于水吸收热,使温度降低,硝酸钾的溶解度减小,可观察到出现更多晶体;
(2)将盛有饱和石灰水的小试管放入盛水的烧杯中,向水中加入某物质后,试管中出现浑浊现象,说明氢氧化钙的溶解度减小了,据氢氧化钙的溶解度随温度的升高而减小,可确定加入的物质使溶液的温度升高,而氢氧化钠固体和浓硫酸溶于水放热,能使溶液温度升高,氧化钙与水反应会放热,能使溶液温度升高.
故答案为:(1)硝酸铵;
(2)试管中的溶液变浑浊,氢氧化钠.
点评 本题难度不大,主要考查了固体溶解度曲线的意义,及根据固体的溶解度曲线来解决相关的问题.


科目:初中化学 来源: 题型:解答题
| 实验步骤 | 实验现象 | 实验结论 |
| 取氢氧化钙样品少量,研细后加适量蒸馏水 充分混合后静置,取少量上层清液,滴加1~2滴无色酚酞试液 | 溶液变成红色 | 该样品还含有氢氧化钙 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
 纸火锅(如图)在巫溪悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;可以吸收汤里多余的杂质与油腻的特性,可维持汤底的清爽,让久煮的食物保留原本的鲜美.
纸火锅(如图)在巫溪悄然兴起,这种纸火锅精巧漂亮,白色的底衬着火锅食料,干净、醒目;纸火锅在使用时无烟、无味;可以吸收汤里多余的杂质与油腻的特性,可维持汤底的清爽,让久煮的食物保留原本的鲜美.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 1:2 | B. | 2:3 | C. | 5:3 | D. | 3:1 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
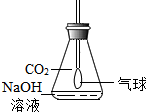 许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.请回答问题:
许多化学反应都伴随着明显的现象.但也有一些观察不到明显现象.请回答问题:查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 铬元素 | B. | 一个铬分子 | C. | 一个铬原子 | D. | 金属铬 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 原子核内质子数为64 | B. | 原子的质量为152 | ||
| C. | 原子核内中子数为89 | D. | 原子的核外电子数为152 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com