

���� ��1�������ڸ��������Ƴɣ������»�Ϳ����е�������Ӧ����������������������������ɫ���Ǻ�ɫ������������Ǻ�ɫ����������»���������绯��ʴ���ɵõ���������Ϊ��ɫ������������Ϊ��ɫ��
��2����ֹ���������ʹ����ˮ������������
��3�����ȸ��ݷ�Ӧԭ���ҳ���Ӧ��������Ӧ���������ݻ�ѧ����ʽ����д���������������д���ɣ�
��4�������������Ǿ��д��Եĺ�ɫ���壬���Խ��Ƶؿ����������������������Ļ���������ᷴӦ�������κ������Σ�
��5������Fe2O3��Fe3O4��FeO��ϡ����ķ�Ӧ�����������������ʵ�鷽�����м��飻
��6������һ����̼�ж�������
��7�����ݷ�Ӧǰ�������仯�������������Fe203����������������ó�������Fe203������������
��8�����������ԣ�Fe2O3��Fe3O4��FeO�ж���CO��Ӧ���Ⱥ�˳��Ȼ���жϷ�Ӧ�¶�800�棨P�㣩ʱ��������ijɷ֣�����������˳���¶��жϹ���������48.0g��Ϊ46.4gʱ�μӷ�Ӧ�����ʣ�Ȼ��д����Ӧ�Ļ�ѧ����ʽ��
��� �⣺��1������������Ϊ��ɫ������������Ϊ��ɫ����b��˵������ȷ��a˵����ȷ��
��2����ֹ���������ʹ����ˮ���������������Բ���Ϳ�ͻ�ˢ��ķ�����
��3����˿��������ȼ��������������������Ӧ�Ļ�ѧ����ʽΪ3Fe+2O2$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4��
��4�����������������ᷴӦ�����Ȼ������Ȼ�������ˮ����ѧ����ʽΪ��Fe3O4+8HCl=FeCl2+2FeCl3+4H2O��
��5�����������Dz�����ˮ�ĺ�ɫ��ĩ�������ᷴӦ�����ԣ�Ҳ���ܱ�������������������ϡ���ᷴӦ��������������������ϡ���������Ȼ�����ˮ���ݴ˿��Լ���������ɣ�����Ϊ��ȡ������Ʒ�ô������������ܱ�����������˵����FeO���ܱ�����������˵�������ۻ�Fe3O4��δ����ȡ������Ʒ����ϡ���ᣬ�������ݣ�˵����������û�в������ݣ�˵����Fe3O4��
��6������CO�ж�������ֱ���ŷţ�Ӧ�����ŷ�β���ĵ����ܿڷ�һյȼ�ŵľƾ��ƣ��������CO����ͨ��ȼ�ճ�����
��7����ó�������Fe203������Ϊx
Fe2O3 +3CO$\frac{\underline{\;����\;}}{\;}$2Fe+3CO2����������
160 112 160-112=48
x l0.0g-7.6g=2.4g
$\frac{160}{x}$=$\frac{48}{2.4g}$
x=8g
�ó�������Fe203����������Ϊ$\frac{8g}{10g}$��100%=80%��
��8������������Fe2O3��Fe3O4��FeO��֪����CO������Ӧʱ��Fe2O3���ȷ�Ӧ��Ȼ��Fe3O4��Ӧ�����FeO��Ӧ������ͼ�����߿�֪�����ȵ�800��ʱ���������ﷴӦ��ȫ����ʱ����ΪFe��
�ʴ�Ϊ��Fe��
�ڹ���������48.0g��Ϊ46.4gʱ����Ӧ�¶�Ϊ400-500�棬��ʱFe2O3��CO��Ӧ��ʧȥ��48g-46.4=1.6g������������Ԫ��Ϊ48��$\frac{48}{160}$=14.4g����Ԫ������=48g-14.4g=33.6g�������������Ԫ������=14.4g-1.6g=12.8g��������Ԫ�ظ�����=$\frac{33.6}{56}$��$\frac{12.8}{16}$=3��4�����Դ�ʱ��ԭ����ΪFe3O4��
��Ӧ�Ļ�ѧ����ʽΪ��3Fe2O3 +CO$\frac{\underline{\;����\;}}{\;}$2Fe3O4+CO2��
�ʴ�Ϊ����1��a����2��ˢ���3��3Fe+2O2$\frac{\underline{\;��ȼ\;}}{\;}$Fe3O4��
��4��Fe3O4+8HCl=FeCl2+2FeCl3+4H2O��
��5��ȡ������Ʒ�ô������������ܱ�����������˵����FeO���ܱ�����������˵�������ۻ�Fe3O4��δ����ȡ������Ʒ����ϡ���ᣬ�������ݣ�˵����������û�в������ݣ�˵����Fe3O4��
��6���������CO����ͨ��ȼ�ճ�������ֹ��������Ⱦ��
��7��80%��
��8��Fe��3Fe2O3 +CO$\frac{\underline{\;����\;}}{\;}$2Fe3O4+CO2��
���� ���⿼�������ʵļ��������������������������ʵ�֪ʶ����Ŀ�ѶȽϴ�ע�����ճ����������ʼ��仯�������ʣ���ȷ���ʼ���������ʵ�鷽������Ʒ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 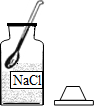 ȡ���Ȼ��ƹ��� | B�� | 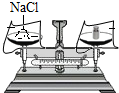 �����Ȼ��ƹ��� | C�� | 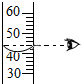 ��ȡˮ����� | D�� | 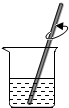 �ܽ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����

| A�� | ֻ�Т� | B�� | ֻ�Т� | C�� | �٢� | D�� | �٢ڢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 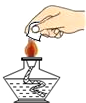 Ϩ��ƾ��� | B�� | 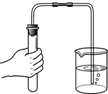 ��������� | C�� |  �μ�Һ�� | D�� | 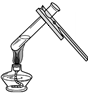 ����Һ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Y��Z��X | B�� | X��Y��Z | C�� | Z��Y��X | D�� | Y��X��Z |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ��֪A��B��C��D��E�dz��л�ѧ�г������������ʣ�����ͬһ��Ԫ�أ����У�ֻ��AΪ���ʣ�B��C���е�Ԫ����ȫ��ͬ��D�����������������ڲ�ͬ�����E��һ����Ҫ�������ϵ���Ҫ�ɷ֣�������һ�������µ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ַ�Ӧ���������ʡ�ԣ�����ش�
��֪A��B��C��D��E�dz��л�ѧ�г������������ʣ�����ͬһ��Ԫ�أ����У�ֻ��AΪ���ʣ�B��C���е�Ԫ����ȫ��ͬ��D�����������������ڲ�ͬ�����E��һ����Ҫ�������ϵ���Ҫ�ɷ֣�������һ�������µ�ת����ϵ��ͼ��ʾ����Ӧ�����Ͳ��ַ�Ӧ���������ʡ�ԣ�����ش��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���Ǻ�ˮ | B�� | ֲ���ͺ����� | C�� | ��;ƾ� | D�� | ���ᱵ��ˮ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com