
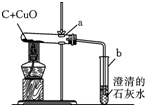
 有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:
有一包黑色粉末可能是由氧化铜和碳粉中的一种或两种物质组成,某学校科学小组为确定其成分,取少量该黑色粉末于烧杯中,加入过量稀硫酸,充分搅拌后观察.如表是实验中可能出现的现象与对应结论,请你填写表中空白处的相关内容:| 现象 | 结论 |
| 溶液呈蓝色,有黑色不溶物 | 含CuO、C |
| 溶液颜色无明显变化,有黑色不溶物 | 只含C |
分析 氧化铜与硫酸可反应生成蓝色的硫酸铜溶液和水,碳和硫酸不反应,据此并结合实验结论、实验现象进行分析;
①碳和氧化铜高温生成铜和二氧化碳,据此书写方程式;
②据反应特点分析反应类型;
③该反应生成二氧化碳,所以可据b中导管口是否产生气泡判断是否完全反应.
解答 解:取少量该黑色粉末于烧杯中,加入过量稀硫酸,若粉末中含有CuO、C,则烧杯内氧化铜与硫酸反应生成硫酸铜溶液,溶液变蓝,碳与硫酸不反应,所以烧杯内还会有黑色不溶物;若溶液颜色无变化,有黑色不溶物,说明黑色粉末中无氧化铜,只有碳;
①碳和氧化铜高温生成铜和二氧化碳,方程式是C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;
②该反应是由单质C和化合物CuO,生成另一种单质Cu和化合物CO2,符合置换反应的特点,属于置换反应;
③该反应生成二氧化碳,所以可据b中导管口是否产生气泡判断是否完全反应;
故答案为:溶液呈蓝色,有黑色不溶物; C;
①C+2CuO $\frac{\underline{\;高温\;}}{\;}$2Cu+CO2↑;②置换;
③b中的导管口不再产生气泡.
点评 本题考查了有关碳的实验探究,了解二氧化碳的性质、氧化铜和硫酸、碳和氧化铜反应实验等知识,才能结合题意正确分析解答.


科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
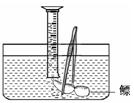 小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占$\frac{1}{4}$,其余主要是二氧化碳(二氧化碳能溶于水)和氮气.探究分两步进行.
小明对妈妈杀鱼时从鱼肚内取出的鳔产生了兴趣,他确定了“探究鳔内气体体积和成分”作为研究性学习的课题.小明通过查阅有关资料获知:这种鱼鳔内氧气约占$\frac{1}{4}$,其余主要是二氧化碳(二氧化碳能溶于水)和氮气.探究分两步进行.| 验证 | 方 法 | 现 象 |
| 鳔内含O2 | 将燃着的木条放入含有鱼鳔内气体的集气瓶中 | 木条能继续燃烧 |
| 鳔内含CO2 | 在含有鱼鳔内气体的集气瓶中加入少量的澄清石灰水 | 石灰水变浑浊 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 加明矾,使海水中的盐分沉淀并淡化 | |
| B. | 利用太阳能,将海水蒸馏淡化 | |
| C. | 将海水通过离子交换树脂,以除去所含的盐分 | |
| D. | 利用半透膜,采用反渗透法而使海水淡化 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.
某化学兴趣小组的同学将一枚洁净的铁钉放入食盐水中(如图所示,装置气密性良好).一段时间后,进行观察.请你一起参与分析,并完成后续实验设计.| 实验步骤 | 实验现象 | 实验结论 |
| 你选用的试剂是: |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 时间 (min) 浓度 条件 | 30%H2O2 | 15%H2O2 | 5%H2O2 |
| 加入agMnO2 | 0.2 | 0.8 | 2.0 |
| 加入agFe2O3 | 7.0 | 9.0 | 16.0 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
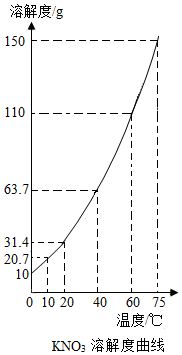 某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:
某固态混合物中含有mgKNO3和若干不溶于水的杂质,将它加入ng水中,在10℃、40℃、75℃时观察,充分溶解后的结果如表:| 温度 | 10℃ | 40℃ | 75℃ |
| 未溶固体 | 261g | 175g | 82g |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com