
| A | 安全常识 | B | 溶解性 |
| 亚硝酸盐--致癌 重金属离子--蛋白质变性 | 氯化钡--易溶于水 碳酸钡--易溶于水 | ||
| C | 物质的性质与用途 | D | 反应规律 |
| 食盐--调味品 碳酸钙--补钙剂 | 湿法炼铜--铁和硫酸铜发生置换反应 食醋除水垢--醋酸和碳酸钙发生复分解反应 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.亚硝酸盐可导致细胞癌变;重金属离子能使蛋白质发生变性;
B.根据氯化钡与碳酸钡的溶解性进行分析;
C.根据食盐有咸味,常用作调味品、碳酸钙与稀盐酸反应进行分析;
D.根据“湿法炼铜”的原理进行分析;根据醋酸除水垢的原理进行分析.
解答 解:A.亚硝酸盐可导致细胞癌变;重金属离子能使蛋白质发生变性;故A正确;
B.氯化钡是重金属盐,易溶于水,碳酸钡难溶于水,故B错误;
C.食盐有咸味,常用作调味品;碳酸钙与胃液的主要成分稀盐酸反应生成可溶性的氯化钙,所以能起到补钙的作用,故C正确;
D.“湿法炼铜”的原理是硫酸铜溶液与铁反应,生成硫酸亚铁和铜,属于置换反应;用醋酸除水壶中的水垢,醋酸与水垢的主要成分碳酸钙生成醋酸钙和水和二氧化碳,属于复分解反应;故D正确;
故选B.
点评 本题主要考查学生运用所学化学知识综合分析和解决实际问题的能力,体现了性质决定用途,用途反映性质的理念,要认真掌握,综合应用.


科目:初中化学 来源: 题型:推断题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | C2H5OH和NaCl 溶液(闻气味) | B. | NaOH溶液和稀H2SO4溶液(酚酞试液) | ||
| C. | Ca(OH)2溶液和NaOH溶液(稀盐酸) | D. | KMnO4 和KClO3 (观察颜色) |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
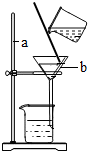 李明同学将浑浊的溪水样品倒入烧杯中,先加入明矾粉末来搅拌溶解,静置一会儿后,然后采用右图过滤装置来除去水中难溶性杂质.试回答:
李明同学将浑浊的溪水样品倒入烧杯中,先加入明矾粉末来搅拌溶解,静置一会儿后,然后采用右图过滤装置来除去水中难溶性杂质.试回答:查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
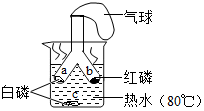 如图所示,将白磷和红磷分装于Y形试管的2个支管中,管口系牢小气球,将2个支管同时伸入相同深度的热水中.
如图所示,将白磷和红磷分装于Y形试管的2个支管中,管口系牢小气球,将2个支管同时伸入相同深度的热水中.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com