

分析 (1)根据恰好完全反应,溶液显中性,进行分析;
(2)根据反应后的溶液是氯化钙溶液,氯化钙和碳酸钠溶液反应生成碳酸钙沉淀;
解答 解:(1)氢氧化钙和稀盐酸反应生成氯化钙和水,所以反应后烧杯中溶液的pH=7;故填:=;
(2)氢氧化钙和稀盐酸反应生成氯化钙和水,图丁中溶液的pH开始小于7,说明图乙实验中,盐酸过量;加入的Na2CO3溶液先与盐酸反应,后与氯化钙反应,丁图中b点时,表示加入的Na2CO3溶液与过量盐酸恰好反应,所对应的溶液中溶质是氯化钙和氯化钠,故填:HCl;CaCl2、NaCl.
点评 本题是一种综合性的题型,将溶液、化学反应和图象融合在一起,有一定的难度,要求比较高.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | CO最多,H2最少 | B. | H2最多,CH4最少 | C. | H2最多,CO最少 | D. | CH4最多,CO最少 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | $\frac{32b}{b-a}$ | B. | $\frac{32b}{a-b}$ | C. | $\frac{16b}{b-a}$ | D. | $\frac{8b}{b-a}$ |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
 向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )
向甲物质中逐渐加入乙物质至过量.若x轴表示加入乙物质的质量,则下列选项与如图不相符合的是( )| 选项 | 甲物质 | 乙物质 | y轴表示的含义 |
| A | 二氧化锰 | 过氧化氢溶液 | 二氧化锰的质量 |
| B | 不饱和蔗糖水 | 加水 | 溶质的质量 |
| C | t℃的水 | 氢氧化钠固体 | 氢氧化钠的溶解度 |
| D | 饱和食盐溶液 | 恒温蒸发溶剂 | 溶液质量分数 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | >7 | B. | <7 | C. | =7 | D. | 无法确定 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
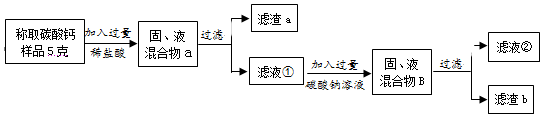
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com