

分析 (1)根据实验室常用仪器的名称和题中所指仪器的作用进行分析;
(2)根据实验室制取二氧化碳是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集进行分析;
(3)①根据用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热进行分析;
根据电石和水反应生成氢氧化钙和乙炔进行分析;
②根据乙炔密度比空气小,难溶于水进行分析;
(4)根据分液漏斗可以控制液体的滴加速度进行分析.
解答 解:(1)通过分析题中所指仪器的作用可知,①是集气瓶,⑧是长颈漏斗;
(2)实验室制取二氧化碳是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集,所以制取二氧化碳的仪器组合是:①②⑦⑧,二氧化碳不具有助燃性,验满的方法是:将燃着的木条放在集气瓶口,如果熄灭,证明已满;
(3)①用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热,所以制取乙炔气体的发生装置与实验室用双氧水制取氧气的发生装置相同,收集满的气体需要用毛玻璃盖住集气瓶口,所以还缺少的仪器名称是毛玻璃片,电石和水反应生成氢氧化钙和乙炔,化学方程式为:CaC2+2H2O=Ca(OH)2+C2H2↑;
②乙炔密度比空气小,难溶于水,所以若用如图装置收集乙炔气体,进气口应为n端;
(4)分液漏斗可以控制液体的滴加速度,所以在上述制取二氧化碳的实验中,可用该分液漏斗置换原来的长颈漏斗,优点是:控制加入稀盐酸的量,节约药品.
故答案为:(1)集气瓶,长颈漏斗;
(2)①②⑦⑧,向上排空气法,二氧化碳的密度比空气大,将燃着的木条放在集气瓶口,如果熄灭,证明已满;
(3)①双氧水,毛玻璃片,CaC2+2H2O=Ca(OH)2+C2H2↑;
②n;
(4)长颈漏斗,控制加入稀盐酸的量,节约药品.
点评 本题主要考查常见气体的发生装置与收集装置的探究,发生装置依据反应物的状态和反应条件选择,收集装置依据气体的密度和溶解性选择.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢氧化钠固体放在烧杯里称量 | |
| B. | 在量筒中稀释浓硫酸 | |
| C. | 排水法收集O2时,看到水槽内导管口有气泡冒出便立即收集 | |
| D. | 用PH试纸测得某溶液的PH为5.5 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题

查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氢气和液氢都可以做燃料--相同物质的分子,化学性质相同 | |
| B. | 用警犬搜救地震中被埋人员--分子在不断运动 | |
| C. | 用水银温度计测量体温--温度升高,原子间隔变大 | |
| D. | 水烧开后把壶盖冲起--温度升高,分子变大 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
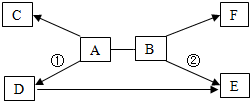 A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).
A~F是初中化学常见的六种物质,它们之间的关系如图所示.“→”表示物质间的转化关系,“-”表示两种物质能相互反应(部分反应物、生成物及反应条件未标出).查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com