

分析 要熟记常见仪器的名称和用途;根据方程式的写法和氧气的密度和溶解性考虑本题;根据氧气的验满方法解答;根据装置的特点以及化合价的求算分析解答即可.
解答 解:(1)据图可以看出,①是长颈漏斗,故填:长颈漏斗;
(2)实验室用高锰酸钾为原料制取一瓶较纯净的氧气,是固体加热型反应,选择A装置制取,排水法收集的氧气纯净,故应选用A装置和C装置,该反应的化学方程式为2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;试管口略向下倾斜是为了防止冷凝水倒流引起试管炸裂;实验中若要调整试管的高度,则应调节a旋钮.若用F装置收集氧气,由于氧气的密度大于空气,则气体从d端进入;用D装置收集氧气,检验氧气已经集满的方法是把带火星的木条放在集气瓶口,木条复燃,证明已满.故填:C;2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;防止冷凝水倒流引起试管炸裂;a;d;把带火星的木条放在集气瓶口,木条复燃,证明已满;
(3)碘酸钾在加热条件下分解生成碘化钾和氧气,方程式为 2KIO3$\frac{\underline{\;\;△\;\;}}{\;}$2KI+3O2↑;碘酸钾中碘元素的化合价为+5,故填:2KIO3$\frac{\underline{\;\;△\;\;}}{\;}$2KI+3O2↑;+5;
(4)过氧化氢在二氧化锰的催化作用下分解生成水和氧气,反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;在该实验设计中,不但可以控制反应的开始和结束,还能控制反应的速率或者便于对催化剂的回收再利用,故填:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;控制反应的速率或者便于对催化剂的回收再利用.
除二氧化锰外,某些金属离子对过氧化氢溶液也有催化作用,如CuSO4溶液中的Cu2+.小明在实验中发现氯化铁(Fe3+和Cl-构成)溶液也能加快过氧化氢的分解速率,要验证是Fe3+对过氧化氢溶液起到了催化作用,需要排除氯离子的可能性,故以下三个实验中,他必须要完成的是在5mL5%的过氧化氢溶液中加入2~3滴氯化钠溶液,几乎无气泡产生,故填:B.
点评 本题考查的是常见气体的实验室制取以及催化剂性质的实验探究,完成此题,可以依据已有的知识进行.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | 盛装固体药品--细口瓶 | B. | 取用硫磺粉末--镊子 | ||
| C. | 取用少量液体--滴管 | D. | 将试管固定在铁架台上--试管夹 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 该元素原子的相对原子质量 | B. | 该元素原子的核电荷数 | ||
| C. | 该元素原子的核外电子数 | D. | 该元素原子的最外层电子数 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A、物质转化 | B、实验记录 |
| ①硬水转化成软水-过滤 ②二氧化碳转化成氧气-光合作用 | ①酚酞溶液中滴入浓氨水,溶液不变色 ②蜡烛火焰分三层,外焰、内焰和焰心 |
| C、爱护水资源 | D、物质鉴别 |
| ①要防止水体污染 ②地球表面水资源丰富,不需节约用水 | ①硫粉、木炭粉-观察颜色 ②空气、氧气、二氧化碳-燃着的木条 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 氮气化学性质稳定--可作保护气 | |
| B. | 氦气密度小--用于飞艇填充气 | |
| C. | 氧气能支持燃烧--可做燃料 | |
| D. | 活性炭具有吸附性--用于冰箱除臭剂 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验步骤 | 实验现象 | 实验结论 |
| ①将等体积的两种无色液体分别加入A、B两个试管中. ②分别向A、B两试管中同时加入等质量(少量)的二氧化锰,观察现象. 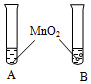 | A试管中无明显现象 B试管中有气泡产生 | (1)A试管中的无色液体是:水; (2)B试管中的无色液体是:过氧化氢溶液; |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题

| A. | 该反应涉及的物质中共有两种元素 | B. | 变化中原子的种类和数目不改变 | ||
| C. | 化学变化中,分子可分,原子不可分 | D. | 该反应为分解反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com