
硫酸锌溶液可以作木材防腐剂.工业上常用红锌矿(主要是ZnO)和稀硫酸为原料制取硫酸锌,化学反应方程式为:ZnO+H2SO4=ZnSO4+H2O.计算:
(1)硫酸锌中锌元素、硫元素和氧元素间的质量比为 .
(2)如果用100g溶质质量分数为1%的硫酸锌溶液配制10%的硫酸锌溶液,需要加入多少克硫酸锌固体.
(3)取50kg某红锌矿与足量稀硫酸充分反应,最后得到80.5kg硫酸锌,则红锌矿中氧化锌的质量分数是多少?(假设红锌矿中的杂质不与稀硫酸反应)
考点:
根据化学反应方程式的计算;有关溶质质量分数的简单计算;元素质量比的计算.
专题:
有关化学式的计算;有关化学方程式的计算;有关溶液溶质质量分数的计算.
分析:
(1)化合物中各元素的质量比,即为化学式中各原子的相对原子质量和的比;
(2)根据配制前后溶液的溶质质量不变分析;
(3)根据硫酸锌的质量计算氧化锌的质量,进而计算红锌矿中氧化锌的质量分数.
解答:
解:(1)硫酸锌中锌元素、硫元素和氧元素间的质量比为:65:32:(16×3)=65:32:48;
(2)设需要加入硫酸锌固体质量为x,
100g×1%+x=(100g+x)×10%
解得:X=10g
(3)设红锌矿中氧化锌的质量为y
ZnO+H2SO4═ZnSO4+H2O,
81 161
y 80.5kg
 =
=
y=40.5kg
红锌矿中氧化锌的质量分数 ×100%=81%
×100%=81%
故答案为:(1)65:32:48;
(2)10g
(3)81%
点评:
本题主要考查学生化学式计算、溶液计算和化学方程式进行计算和推断的能力,计算时要注意规范性和准确性.


 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了两个实验:
①CuSO4溶液与NaOH溶液、②CuSO4溶液与BaCl2溶液反应。实验结束后将两次实验中的废液倒入同一个干净的烧杯中,充分混合后过滤,得到滤液呈无色。
(1)写出实验②发生反应的化学方程式: ▲ 。
(2)取少量滤液于试管中,滴入紫色石蕊试液,石蕊溶液为紫色,则滤液呈 ▲ 性(填
“酸”、“中”、“碱”)。 废液在烧杯中混合后,肯定发生的化学反应的方程式:
▲ 。
(3)该小组的同学对滤液中溶质的成分继续进行了如下探究实验:
【提出问题】滤液中溶质的成分是什么?
【作出猜想】小红认为:只含氯化钠;
小明认为:可能含有硫酸钠、氯化钠和氯化钡;
小亮认为:可能含氯化钠和氯化钡;
你认为:还可能是 ▲ (写一种猜想)。
【讨论】你认为小红、小明、小亮三位同学中谁的猜想明显不合理?为什么?
▲
【实验探究】
| 实验操作 | 实验现象 | 实验结论 |
| 实验A:取少量滤液于试管中,加入 适量纯碱溶液,振荡。 | 无明显现象 | 滤液中不含 ▲ |
| 实验B:取少量滤液于试管中,加入适量硝酸钡溶液,振荡。 | 产生白色沉淀 | 滤液中含有 ▲ |
【交流拓展】a.要使蓝色溶液变成无色,除了加入NaOH等碱性溶液外,还可以在蓝色溶液中加入足量的 ▲ 。
b.在盛有100g氢氧化钠溶液的大烧杯中缓缓加入硫酸铜溶液,反应生成沉淀的质量与加入硫酸铜溶液质量的关系如图所示:求恰好完全反 应时,所得溶液中溶质的 质量分数?(精确到0.1% )
应时,所得溶液中溶质的 质量分数?(精确到0.1% )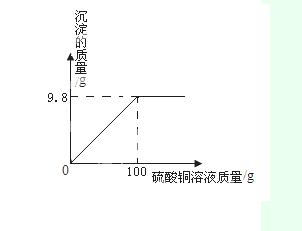
查看答案和解析>>
科目:初中化学 来源: 题型:
将一定质量的铁和氧化铜的混合物粉末放入足量稀盐酸中,充分反应后产生气体0.4g,并得到残留固体6.4g.则原混合物粉末的质量是( )
|
| A. | 8.0g | B. | 11.2g | C. | 16.0g | D. | 24.8g |
查看答案和解析>>
科目:初中化学 来源: 题型:
为测定某氨肥中硫酸铵的纯度(即质量分数)是否与如图标签相符,小林取一定量该氨肥样品与烧杯中配成溶液与足量氯化钡溶液反应,记录有关数据如下表
| 反应前 | 反应后 |
|
| 烧杯和样品溶液总质量 | 氯化钡溶液质量 | 过滤后烧杯和溶液总质量(滤液的损失忽略不计) |
| 45g | 55g | 76.7g |
【反应的化学方程式为(NH4)2SO4+BaCl2═BaSO4↓+2NH4Cl4,其他成分能溶于水但不参加反应】
(1)反应共生成BaSO4的质量为 g
(2)若所取氨肥样品的质量为15g,试通过计算确定氨肥中硫酸铵的纯度是否与标签相符.(请写出计算过程)
(3)反应前后,溶液中硫元素的质量 (填“不变”、“增大”或“减小”)

查看答案和解析>>
科目:初中化学 来源: 题型:
菱铁矿(主要成分是FeCO3)是炼铁的原料.现取20.0g菱铁矿,向其中加入足量稀硫酸,充分反应,测得固体质量与所加稀硫酸的质量关系如图所示
已知:①FeCO3+H2SO4=FeSO4+CO2↑+H2O ②菱铁矿中杂质不参加反应,且难溶于水.
请计算:
(1)20.0g菱铁矿中FeCO3的质量为 g
(2)列式计算所用稀硫酸的溶质质量分数(结果准确到0.1%)

查看答案和解析>>
科目:初中化学 来源: 题型:
镁铜合金常用作飞机天线等导电材料,现取某镁铜合金10g放入烧杯中,加入足量稀硫酸充分反应后,测得剩余固体的质量是6.4g,请计算:
(1)该镁铜合金中镁的质量为 g
(2)生成H2的质量.
查看答案和解析>>
科目:初中化学 来源: 题型:
.实验室现有一种含有氯化钠的纯碱固体样品。某化学兴趣小组的同学在老师的指导下,利用如下图所示装置(部分固定装置已略去)进行实验,测定其中纯碱的含量,并证实二氧化碳能与氢氧化钠发生化学反应。已知,该装置气密性良好,氢氧化钠溶液过量。
 探究过程如下:
探究过程如下:
Ⅰ. 称量纯碱样品质量记为 m,装置B及其中试剂的总质量为 m 1,
Ⅱ. 将质量为m的样品装入装置A中,关闭止水夹K2,打开止水夹K1.向样品中加入足量的稀硫酸,充分反应后,观察到C装置中的澄清石灰水不变浑浊。再次称B装置的总质量为m2.
Ⅲ.关闭止水夹K1,打开止水 夹K2,使B装置与空气连通.向D装置内加入足量的稀盐酸(溶液浸没长颈漏斗下端管口)充分反应,观察现象。请回答:
夹K2,使B装置与空气连通.向D装置内加入足量的稀盐酸(溶液浸没长颈漏斗下端管口)充分反应,观察现象。请回答:
(1)利用A装置制取二氧化碳的发生装置与实验室用氯酸钾制取氧气的
发生装置 (填“相同”或“不同”)
(2)二氧化碳与氢氧化钠反应的化学方程式为 。
(3)依据实验所得数据,该组甲同学得出计算样品中纯碱含量的式子为 53(m2- m1)/22 m,通过误差分析,乙同学发现所用数据不可靠。造成该数据不可靠的原因及其对计算结果的影响是:
①没有事先排走空气中的二氧化碳,导致计算结果偏大。
② 。(任选一个因素)
(4)证实二氧化碳与氢氧化钠溶液发生了反应的现象是 。
(5)实验结束后,B装置溶液中含有的溶质可能有多种情 况,任意写出其中的一种情况 。
况,任意写出其中的一种情况 。
查看答案和解析>>
科目:初中化学 来源: 题型:
常温下,将100 mL的空气通过足量灼热的铜网,充分反应后,恢复到常温,余下气体的体积约为( )
A.80 mL B.60 mL C.40 mL D.20 mL
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com