
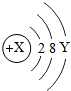 为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-.
为某元素的粒子结构示意图,若为原子,则X-Y等于10.若X-Y等于8,则该粒子的符号是S2-. 分析 (1)根据原子核电荷数=核内质子数=核外电子数,可知粒子中,属于原子的有哪些;根据阴离子的核内质子数<核外电子数,可知粒子中,属于阴离子的有哪些;掌握元素的概念:具有相同核电荷数(核内质子数)的一类原子的总称进行分析;
(2)根据化合价表示原子之间互相化合的数目和元素最外层电子数进行分析解答;
(3)根据原子中质子数=核外电子数,离子中,质子数不等于核外电子数进行分析.
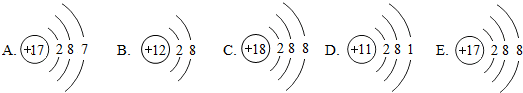
解答 解:(1)根据最外层有8个电子的属于稳定结构,所以电子层结构相同的是BCE,根据相同核电荷数(核内质子数)的一类原子的总称为元素,则为同种元素,所以表示同一种元素的是AE,根据阳离子的核内质子数>核外电子数,所以表示阳离子的是B,其离子符号Mg2+;
(2)M元素原子最外层有7个电子,在化学反应中容易得到1个电子,从而带上1个单位的负电荷,故M元素的化合价为-1价;N元素的原子最外层有2个电子,在化学反应中容易失去2个电子,从而带上2个单位的正电荷,故N元素的化合价为+2价;根据化合物中正负化合价的代数和为0,它们形成化合物的化学式为NM2;
(3)因为该微粒是原子,质子数等于核外电子数,所以X=10+Y,X-Y=10;
X-Y=8,所以X=Y+8,所以X=16,该微粒是硫离子,粒子的符号是S2-.
故答案为:(1)BCE,AE,B,Mg2+;
(2)NM2;
(3)10,S2-.
点评 本题难度不大,考查学生对粒子结构示意图及其意义的理解,明确粒子中核内质子数和核外电子数之间的关系是解题的关键.


科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| 实验操作 | 实验现象 | 实验结论 |
| 取少量滤液于试管中,加入足量CaCl2溶液 | 有白色沉淀产生且红色不消失 | 猜想③成立 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 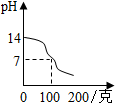 | B. | 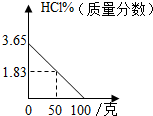 | ||
| C. | 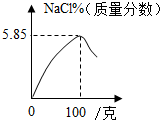 | D. | 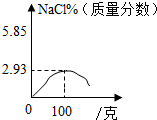 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com