
| 名称 | 新鲜肉 | 次鲜肉 | 变质肉 |
| pH | 5.8~6.2 | 6.3~6.6 | >6.7 |
| A. | 逐渐变弱 | B. | 保持不变 | C. | 逐渐变强 | D. | 无法确定 |
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:选择题
| A. | CH4 | B. | C2H2 | C. | C3H8 | D. | C8H18 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
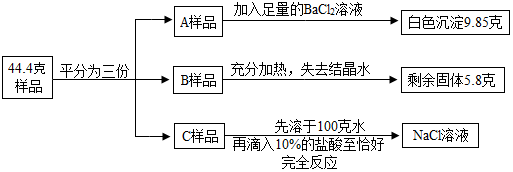
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
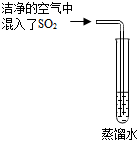 已知 CO2的饱和溶液常温下pH不小于 5.6.通常空气中CO2的含量大于SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.
已知 CO2的饱和溶液常温下pH不小于 5.6.通常空气中CO2的含量大于SO2的含量,但人们反而将空气中的 SO2认定为形成酸雨的主要原因之一.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 紫色石蕊 | B. | 无色酚酞 | C. | Na2CO3 | D. | AgNO3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 方案A | 方案B |
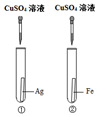 | 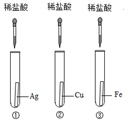 |
| (1)实验中发生反应的化学方程式为Fe+CuSO4=FeSO4+Cu. (2)实验中观察到的现象是①中无明显变化,②中铁片表面覆盖一层红色物质,溶液由蓝色变成浅绿色. (3)该方案能(填“能”或“不能”)验证三种金属的活动性. | (1)实验中发生反应的化学方程式为Fe+2HCl=FeCl2+H2↑. (2)实验中观察到的现象是①②中均无明显变化,③中有气泡冒出,溶液由无色变成浅绿色. (3)该方案不能(填“能”或“不能”)验证三种金属的活动性. |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
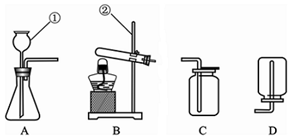
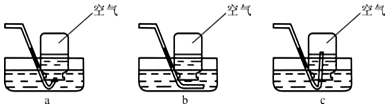
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.
钛(Ti)因为具有许多神奇的性能而越来越引起人们的关注.| Ti | Mg | Ag | |
| 实验现象 | 产生气泡速度缓慢 | 产生气泡速度快 | 无任何现象 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com