
| A. | 消耗等质量的H2SO4 | B. | 生成等质量的ZnSO4 | ||
| C. | 消耗等质量的CuO | D. | 所有反应的条件相同 |
分析 根据化学方程式的意义,由两种途径的反应方程式及制取过程中的注意事项,根据要制得等质量的铜,分析有关量的关系;根据反应物、生成物的种类既反应的特点分析反应的类型.
解答 解:(1)第一种方案:CuO+H2SO4=CuSO4+H2O,CuSO4+Zn=ZnSO4+Cu.说明生成64克铜需要65克锌和160克硫酸铜,同时生成硫酸锌的质量为161克;生成160克硫酸铜需要80克氧化铜和98克硫酸;
(2)第二种方案:Zn+H2SO4=ZnSO4+H2↑,H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O.根据氢气还原氧化铜的实验注意事项可知,氢气要通入一段时间后才开始加热反应,因此氢气是过量的.所以生成64克铜需要氧化铜的质量等于80克,需要氢气的质量大于2克;生成大于2克的氢气需要锌的质量大于65克,需要硫酸的质量大于98克,同时生成硫酸锌的质量大于161克;综合上述分析可知:
A、消耗H2SO4的质量不相等.故A错误;
B、生成ZnSO4的质量不相等.故B错误;
C、消耗等质量的CuO.故C正确;
D、所有反应的条件不同.故D错误.
故选C.
点评 解答本题的关键是掌握氢气还原氧化铜实验的操作方法,即氢气是过量的,所以需要硫酸和锌的质量也过量的.


 新思维假期作业暑假吉林大学出版社系列答案
新思维假期作业暑假吉林大学出版社系列答案 蓝天教育暑假优化学习系列答案
蓝天教育暑假优化学习系列答案科目:初中化学 来源: 题型:选择题
 如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )
如图是某广口瓶的标签,已经部分被污损和腐蚀.小明想探究其成分,他取一支洁净的试管,加入少量广口瓶中的固体,滴入少量盐酸,有无色无味气泡产生.该气体能使澄清石灰水变浑浊,则该固体( )| A. | 一定是Na2CO3 | B. | 可能是Na2CO3,也可能是NaHCO3 | ||
| C. | 一定是NaHCO3 | D. | 一定是Na2CO3和NaHCO3的混合物 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
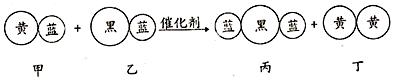
| A. | 该反应中共有三种元素 | B. | 乙和丙中所含的元素种类相同 | ||
| C. | 乙和丙都是化合物 | D. | 甲和丁中同种元素的化合价相等 |
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
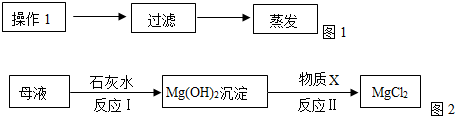
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com