5.6g铁和铜的混合物与足量的稀硫酸反应,生成氢气的质量可能是( )
A.0.2g
B.0.18g
C.0g
D.0.4g
【答案】
分析:铁会和硫酸反应;铜不会和硫酸反应;写出化学方程式,假设5.6G全部是铁,代入铁的质量计算出氢气的质量,这是氢气质量的最大值.
解答:解:铁会和硫酸反应,铜不会和硫酸反应;假设5.6g全部是铁,与硫酸反应生成氢气的质量为x,
Fe+H
2SO
4 ═FeSO
4+H
2↑
56 2
5.6g x
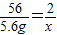
x=0.2g
因为5.6g是铁和铜的混合物,因此氢气的质量一定小于0.2g,因为5.6g是铁和铜的混合物,只要有铁,则一定会产生氢气,因此氢气的质量一定不为0.
故选B
点评:本题采用极端假设法,求出氢气的最大值,然后分析氢气质量的范围.

 星级口算天天练系列答案
星级口算天天练系列答案