
| 编号 | 0.25%淀粉溶液(ml) | 蒸馏水(ml) | 0.9%Na2SO4溶液(ml) | 0.9%CuSO4溶液(ml) | 唾液溶液(ml) | 加入碘液 3滴后现象 |
| 1 | 3 | 2 | - | - | - | 变蓝 |
| 2 | 3 | 1 | - | - | 1 | 不变蓝 |
| 3 | 3 | - | 1 | - | 1 | 不变蓝 |
| 4 | 3 | - | - | 1 | 1 | 变蓝 |
分析 淀粉遇碘变蓝色;
唾液淀粉酶能够加快淀粉的分解;
根据实验现象可以判断相关方面的问题.
解答 解:(1)由1、2号试管对照可知,1中淀粉没有分解或没有完全分解,2中淀粉完全分解,因此唾液淀粉酶对淀粉的分解起到促进作用.
故填:唾液淀粉酶对淀粉的分解起到促进作用.
(2)由上表4中实验结果可知,淀粉没有分解或没有完全分解,说明重金属会影响酶的催化作用.
故填:会.
(3)王刚在试管3中滴加0.9%Na2SO4的目的是验证钠离子能否影响酶的催化作用.
故填:验证钠离子能否影响酶的催化作用.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.


 出彩同步大试卷系列答案
出彩同步大试卷系列答案科目:初中化学 来源: 题型:填空题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
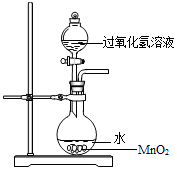 用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:
用过氧化氢制氧气时,有同学对事先在烧瓶中加水产生了疑问.他提出了猜想:| 实验 | 1 | 2 | 3 | 4 | 5 |
| 过氧化氢溶液溶质质量分数 | 1% | 3% | 5% | 10% | 15% |
| MnO2粉末用量/克 | 0.5 | 0.5 | 0.5 | 0.5 | 0.5 |
| 收集到500mL气体时所用时间/秒 | 560 | 186 | 103 | 35 | 12 |
| 反应后液体温度/℃ | 26 | 38 | 43 | 59 | 71 |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
| A | B | C | D | E | |
| 所放废电池型号 | 1号 | 2号 | 5号 | 7号 | 对照 |
| 金鱼成活时间(天) | 1 | 7 | 15 | 18 | 至今 |
| A | B | C | D | E | |
| 所放废电池型号 | 1号 | 1号 | 1号 | 1号 | 1号 |
| 满江红数量(g) | 0 | 40 | 80 | 120 | 160 |
| 溶解氧(mg/L) | 2.25 | 2.94 | 3.65 | 4.12 | 5.06 |
| 铅(mg/L) | 0.135 | 0.134 | 0.106 | 0.084 | 0.029 |
| 金鱼成活时间(天) | 1 | 8 | 13 | 17 | 至今 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 在点燃蜡烛时,小红发现有一根烛芯沾有食盐的蜡烛比普通蜡烛燃烧的时间长一些.请你与小红一起探究,并回答相关问题.
在点燃蜡烛时,小红发现有一根烛芯沾有食盐的蜡烛比普通蜡烛燃烧的时间长一些.请你与小红一起探究,并回答相关问题.| 食盐质量(g) | 0 | 0.1 | 0.5 | 0.7 | 0.9 | 1.0 |
| 燃烧时间(分钟) | 10 | 15 | 18 | 23 | 25 | 27 |
| 燃烧稳定性 | 正常 | 正常 | 正常 | 正常 | 易灭 | 极易灭 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 某学习小组探究氢氧化钙溶液的化学性质,并做了延伸探究.
某学习小组探究氢氧化钙溶液的化学性质,并做了延伸探究.| 方案 | (1) | (2) | (3) |
| 实验操作 | 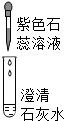 | 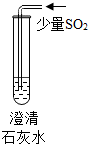 |  |
| 现象 | 溶液变为蓝色 | 澄清石灰水变浑浊 | 红色褪为无色 |
| 结论或解释 | 氢氧化钙溶液能使石蕊等酸碱指示剂变色 | 氢氧化钙溶液能与某些非金属氧化物反应生成盐和水.二氧化硫与澄清石灰水反应的化学方程式是 SO2+Ca(OH)2═CaSO3↓+H2O | 氢氧化钙溶液能与酸发生中和反应 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | 物理变化过程中,分子本身发生了变化 | |
| B. | 分子是由原子构成的 | |
| C. | 原子是化学变化中的最小微粒 | |
| D. | 化学反应的实质是原子的重新组合 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | H+、Na+、Cl-、NO3- | B. | H+、SO42-、Cl-、NO3- | ||
| C. | K+、Na+、Cl-、NO3- | D. | Ca2+、SO42-、Cl-、NO3- |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 验证猜想 | 对比实验操作 | 实验现象 | 实验结论 |
| 猜想① | 将蜡烛分别在空气和纯氧中点燃 | 蜡烛在 氧气中燃烧 比在空气中燃烧更剧烈 | 氧气浓度 越大 燃烧越剧烈 |
| 猜想② | 将质量相同的木炭块 和木炭粉分别放在 氧气中燃烧 | 木炭粉比木炭块 燃烧 更剧烈 | 接触面积 越大 燃烧越剧烈 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com