
为了测定某石灰石样品中碳酸钙的质量分数,某学习小组取来一些石灰石样品,并取稀盐酸200g,进行了四次实验,结果如下:
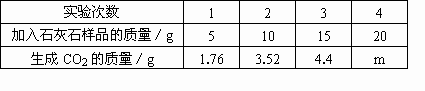
(1)哪几次反应中石灰石有剩余?
(2)第4次实验中m的值是多少?
(3)求该石灰石样品中碳酸钙的质量分数?
|
答:(1)第3、4两次 (2)4.4 (3)原石灰石样品中CaCO3的质量分数为80%. 第一次5g石灰石完全反应、生成1.76g CO2.第2次石灰石为10g,生成CO2 3.52g,(石灰石增加1倍,生成的CO2也增加1倍)石灰石也完全反应.第3次石灰石为第1次的3倍,生成的CO2小于第1次的3倍,故第3、4次石灰石有剩余.故第4次实验中生成的CO2也应为4.4g. (若第3次石灰石也完全反应,则应生成CO2 5.28g,现只生成CO2 4.4g) 解:设石灰石样品中CaCO3的质量为x CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 x 1.76g (按第2次实验中的数据计算,其结果相同) |


科目:初中化学 来源: 题型:
为了测定某石灰石样品中碳酸钙的质量分数,某学生取稀盐酸200g,平均分成四组进行实验,结果如下:
|
查看答案和解析>>
科目:初中化学 来源:2012-2013学年江苏省南京市江宁区中考一模化学试卷(解析版) 题型:推断题
对牙膏的探究要用到许多化学知识。
(1)用作牙膏摩擦剂的轻质碳酸钙,工业上常用石灰石来制备,某实验小组同学设计了2种转化流程,如下图1所示.

请回答下列问题:
a.小王同学主张用流程①、②、④和操作Ⅱ的设计,认为其工艺简单。
请写出反应①和④的化学方程式:① ;④ ;
b.操作Ⅱ包括搅拌、 、洗涤、干燥等工序。
c.小李同学认为流程①、②、③和操作I比小王的主张更好,其理由是: ;
操作I包括搅拌和微热等工序。
(2)该实验小组为了测定某石灰石样品中碳酸钙的质量分数,取25g石灰石样品放在烧杯中,然后向其中逐滴加入一定量某质量分数的稀盐酸,使之与样品充分反应(杂质不参加反应)。随着反应进行,加入稀盐酸的质量与反应得到气体的质量变化关系如图2所示,请完成下列计算内容:
①样品中碳酸钙的质量分数是多少?
②所用稀盐酸溶质的质量分数是多少?
查看答案和解析>>
科目:初中化学 来源: 题型:
为了测定某石灰石矿样的纯度(其中所含杂质不与酸反应),某同学按如下流程进行实验:用盐酸溶解矿样→干燥所得气体→用NaOH溶液吸收气体→根据NaOH溶液的增重量计算矿样的纯度。实验过程中所取矿样的质量为10g。实验装置如下图所示:
 |
(1) A为溶解矿样的装置,若已经准备了长颈漏斗、双孔橡胶塞、导气管,为了完成溶解至少还需要的实验仪器是_____________________________
(2) A中发生反应化学方程式______________________________________
(3) B中所盛的试剂是______________________________________
(4)根据上述装置进行实验,下列情况会使实验结果产生偏差的是______________
①实验开始A、B装置以及导气管内残留有少量空气
②进入C装置的气体中还混有少量HCl气体
③气体通过速度过快,CO2来不及被NaOH溶液全部吸收
④实验结束时,系统内还残留有少量CO2气体
(5)将插入溶液的管子的下端改成具有多孔的球泡(图中的D),有利于提高实验的准确度,其理由是_____________________________________________________________
(6)改进实验装置并进行正确操作可以准确测出矿样的纯度,若此时C装置在实验前后其质量增加了3.6 g,则该矿样的纯度为______________
查看答案和解析>>
科目:初中化学 来源: 题型:
为了测定某石灰石中碳酸钙的质量分数(假设杂质不参加反应,且不溶于水),某兴趣小组设计如下实验方案:①称取10g石灰石样品,②高温煅烧至质量不再改变,③把剩余固体放在空气中冷却至室温,④称得剩余固体的质量为6.04g。
①在方案中产生二氧化碳的质量为 g,其物质的量为 mol。
②根据方案计算石灰石中碳酸钙的质量分数(根据化学方程式列式计算)。
③指出该实验方案中一处明显的不足并说明原因 ![]() 。,
。,
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com