
【题目】下列实验操作与图象关系对应正确的是( )
选项 | A | B | C | D |
操作 | NaOH溶液中不断加水稀释 | 水电解生成氢气与氧气 | 向等量的稀硫酸中加入足量的镁、铝 | 用等质量、等质量分数的过氧化氢溶液制取氧气 |
图象 |
|
|
|
|
A.AB.BC.CD.D
 阅读快车系列答案
阅读快车系列答案科目:初中化学 来源: 题型:
【题目】如图所示,A-G是初中化学常见的物质,其中B、C、D、E、F都是氧化物,图中“→”表示转化关系。“-”表示相互能反应,已知A是人体胃液中含有的酸,G是最轻的气体,B能作气体肥料,E是某些食品干燥剂的主要成分,D与A反应会生成黄色溶液,请回答:
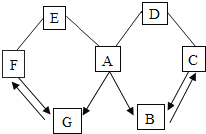
(1)F的化学式为______。
(2)E的俗名是______。
(3)C和D反应时的现象是______。
(4)A和D反应的化学方程式为______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】“碳捕捉技术”是通过一定的方法,将工业生产中产生的二氧化碳分离出来并加以利用。某校科研小组的同学设计用氢氧化钠溶液来“捕捉”二氧化碳,其基本过程如下(部分条件及物质未标出)。
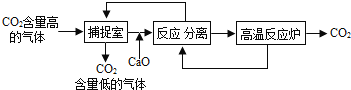
请回答下列有关问题:
(1)“捕捉室”中发生反应的化学方程式为:___________________;
(2)在整个“捕捉”过程中,可以循环利用的物质是_____;
(3)下列有关叙述中错误的是_____(填序号)。
A 该技术可有效减少碳排放
B “反应分离”过程中,分离物质的基本操作时蒸发结晶和过滤
C 能耗大是该技术的一大缺点
D “捕捉”到的二氧化碳可用于生产尿素、甲醇、碳酸氢铵和纯碱等
查看答案和解析>>
科目:初中化学 来源: 题型:
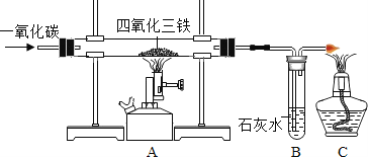
【题目】在实验室里,可以利用如图装置制得铁。
(1)A处玻璃管内所发生反应的化学方程式为______。
(2)B处可观察到的现象是______;C处酒精灯的作用是______
(3)待四氧化三铁完全反应后,停止加热A处,在断开A、B之前应继续通入一氧化碳至A处玻璃管冷却。若不继续通入一氧化碳。可能出现的后果是______。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】用“侯氏制碱法” 制取的纯碱中常常含有少量的氯化钠。为了测定某纯碱样品中碳酸钠的质量分数,小雯同学称取该样品 5.6g 加入到烧杯中,再向烧杯中滴加稀盐酸至 100g 时,恰好完全反应,称得烧杯中的溶液质量为103.4g。求:
(1) 完全反应产生二氧化碳的质量是___________________________g。
(2) 100g 稀盐酸溶液中溶质的质量分数。___________________________
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学学习离不开化学变化,变化实现物质间的相互转化:
(1)Ca(OH)2变质
①请写出Ca(OH)2变质的原因______(用化学方程式表示)。
(2)定性研究Ca(OH)2变质程度
②请设计实验确定Ca(OH)2的变质程度,写出操作、现象及结论______。
(3)定量研究Ca(OH)2变质程度
③配制稀盐酸:计算配制300g质量分数为5%的盐酸,需要质量分数为30%的盐酸______g。
配制过程中,除烧杯、玻璃棒、量筒外,还需用到的玻璃仪器是______。若量取30%的盐酸时俯视读数,所配制的盐酸质量分数______5%(填大于、小于)。
④实验测定:称取40.0g样品置于烧杯中,加入足量稀盐酸充分反应,烧杯总质量与反应时间的关系如表所示:
反应时间/min | 0 | t1 | t2 | t3 | t4 |
烧杯总质量/g | 150.0 | 147.8 | 145.6 | 145.6 | 145.6 |
请计算该样品中Ca(OH)2的质量分数。_____
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】化学是认识、改造和应用物质的科学。从海水中提取镁、制“碱”,都体现了人类改造物质的智慧。结合下列流程图(其中部分操作和条件已略去),请回答相关问题:
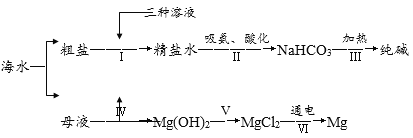
(1)提纯物质常用转化的方法,就是将杂质转化为沉淀或气体而除去。粗盐中含有氯化镁、硫酸钠、氯化钙等可溶性杂质,通过步骤Ⅰ,再利用过滤操作进行除杂。步骤Ⅰ加入下列三种溶液的先后顺序为_____(填字母序号);
a.稍过量的Na2CO3溶液 b.稍过量的BaCl2溶液 c.稍过量的NaOH溶液
(2)母液中有MgCl2,却经历了步骤Ⅳ、Ⅴ的转化过程,其目的是_____;
(3)步骤Ⅱ中先向饱和食盐水中通入氨气,有利于二氧化碳的吸收,这样做的目的是_____,写出该反应的化学方程式_____;
(4)化学变化是改造物质的重要途径。上述流程图中没有涉及的基本反应类型是_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】有A、B、C、D四个烧杯中分别盛有质量相等的同种溶剂,在相同的温度下,向四个小烧杯中分别加入200g、150g、100g、50g某溶质,充分溶解后,如图所示。请回答:
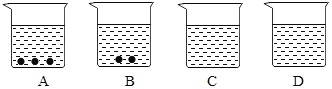
(1)_______(填序号,下同)中盛的一定是饱和溶液;______中盛的一定是不饱和溶液,______中盛的可能是饱和溶液。
(2)四个烧杯中溶液的溶质质量分数由小到大的顺序是:______。
(3)若固体溶质是硝酸钾,对A、B两个烧杯同时升高温度(均匀进行),固体物质先消失的是____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】某化学兴趣小组的同学在老师的指导下,对一瓶出现变质硬化的氢氧化钙固体变质程度进行探究,测定3g样品中含有杂质的质量,设计实验装置(气密性良好)如图1所示.

(1)取3克部分变质的氢氧化钙样品放入烧瓶中.滴入稀盐酸,当观察到 (填实验现象),停止滴加稀盐酸;
(2)实验结束后,量简内进入水的体积如图2所示,其演数为165mL,已知在该实验条件下,生成气体的密度为2gL﹣1,则生成C02气体的质量为 ;(精确到 0.01)
(3)请计算3克变质的氢氧化钙祥品中杂质的质量.(精确到0.01)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com