
| ||
| ||
| ||


科目:初中化学 来源: 题型:

| A、若用排空气法往装置内收集CO2时,气体应从A端通入 |
| B、若用排空气法往装置内收集H2时,气体应从A端通入 |
| C、若用水将此装置中的O2排出,水应从B端进入 |
| D、若要除去O2中少量的CO2可在此装置中装入过量的Ca(OH)2溶液,气体从B端通入 |
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、用氢气灌装氢气球,是利用氢气的可燃性 |
| B、氮气用来保护粮食,是利用氮气常温下化学性质稳定 |
| C、氧气具有助燃性,支持碳的燃烧 |
| D、稀有气体充入霓虹灯,是利用稀有气体通电能发出不同颜色的光 |
查看答案和解析>>
科目:初中化学 来源: 题型:
查看答案和解析>>
科目:初中化学 来源: 题型:
| A、分子和原子在化学反应里都能生成新的分子和原子 |
| B、由同种元素组成的物质称为纯净物 |
| C、含有氧元素的化合物称为氧化物 |
| D、分子、原子、离子都是构成物质的粒子 |
查看答案和解析>>
科目:初中化学 来源: 题型:
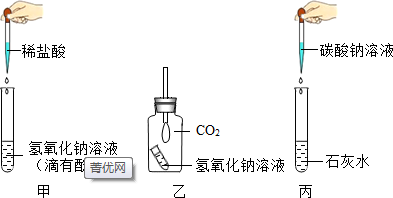
查看答案和解析>>
科目:初中化学 来源: 题型:
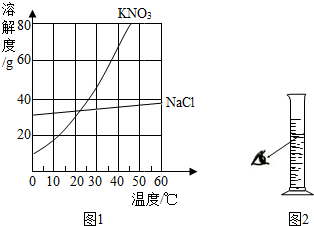 小梅帮助老师配置KNO3的饱和溶液,以备全班实验使用,此实验室温度为25℃,老师提供的药品是含有少量氯化钠的硝酸钾固体.
小梅帮助老师配置KNO3的饱和溶液,以备全班实验使用,此实验室温度为25℃,老师提供的药品是含有少量氯化钠的硝酸钾固体.查看答案和解析>>
科目:初中化学 来源: 题型:
| 温度/℃ | 10 | 20 | 30 | 40 | 50 | 60 | 70 |
| NaCl的溶解度 | 35.8 | 36.0 | 36.3 | 36.6 | 37.0 | 37.3 | 37.8 |
| KNO3的溶解度 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110.0 | 138.0 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com