
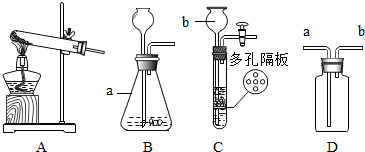
分析 ①据常用仪器回答;
②装置C适用于固体和液体常温混合制取气体;
③(Ⅰ)根据信息提供的制取氨气的反应物的状态和反应条件选择发生装置:固体加热型和固液常温型;根据氨气的密度和溶解性确定进气口;
(Ⅱ)根据氨气的性质分析对酚酞试液的作用;
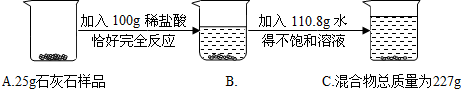
④(Ⅰ)据物质的质量和物质的量之间的关系解答;
(Ⅱ)据二氧化碳的质量结合方程式计算碳酸钙的质量,进而计算碳酸钙的质量分数.
解答 解:①标号仪器分别是锥形瓶和长颈漏斗;
②装置C适用于固体和液体常温混合制取气体;
③(Ⅰ)用加热氯化铵和氢氧化钙的固体混合物制取氨气,因此制取氨气的发生装置的特点是固体加热型的A装置;因为氨气(NH3)是一种密度比空气小的气体,所以应从短管进气,将空气挤压到集气瓶上部排出;
(Ⅱ)因为氨气极易溶于水,且水溶液显碱性,故看到的现象是:滴有酚酞的水进入集气瓶中,酚酞试液变成红色;
④(Ⅰ)根据质量守恒定律可知:生成二氧化碳的质量是:25g+100g+110.8g-227g=8.8g,物质的量是$\frac{8.8g}{44g/mol}$=0.2mol;
(Ⅱ)设样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
所以样品中碳酸钙的质量分数是:$\frac{20g}{25g}$×100%=80%;
答:石灰石样品中碳酸钙的质量分数是80%;
故答案为:①锥形瓶;长颈漏斗
②反应物是固体和液体,反应不需要加热;
③(Ⅰ)A;h;(Ⅱ)滴有酚酞的水进入集气瓶中,酚酞试液变成红色;
④(Ⅰ)0.2;
(Ⅱ)设样品中碳酸钙的质量为x
CaCO3+2HCl=CaCl2+H2O+CO2↑
100 44
x 8.8g
$\frac{100}{x}$=$\frac{44}{8.8g}$
x=20g
所以样品中碳酸钙的质量分数是:$\frac{20g}{25g}$×100%=80%;
答:石灰石样品中碳酸钙的质量分数是80%.
点评 本题考查知识较为综合,既考查了装置选取,又考查了方程式计算等知识,能较好考查学生分析、解决问题的能力.


科目:初中化学 来源: 题型:解答题
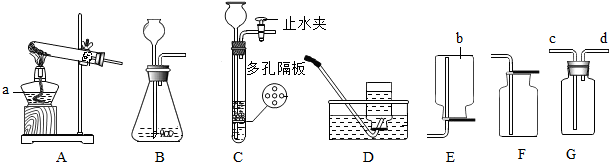
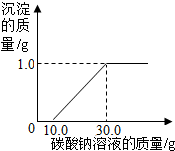 【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.
【拓展与应用】①若实验证明了你的猜想是正确的,向废液中加入过量的碳酸钙,反应完成后过滤,即可得到只含CaCl2一种溶质的溶液.查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Na2SO4、NaCl、BaCl2 | B. | H2SO4、NaCl、KNO3 | ||
| C. | CuSO4、KCl、HCl | D. | HCl、NaOH、NaCl |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| 选项 | 目的 | 方案 |
| A | 除去木炭粉中的氧化铜 | 在空气中充分燃烧 |
| B | 分离NaCl和CaCO3的混合物 | 加足量稀盐酸,蒸发 |
| C | 区分稀盐酸和稀氢氧化钠溶液 | 分别测溶液的pH |
| D | 鉴别化肥NH4Cl和NH4NO3 | 取样,加熟石灰研磨 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:初中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com