
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | 蓝色 | 蓝色 |
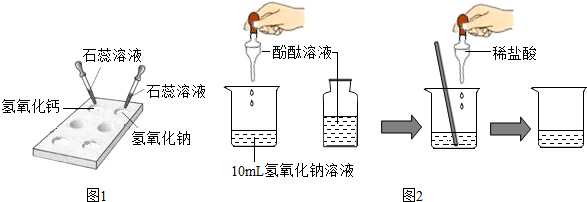
分析 根据紫色石蕊试液遇碱性溶液变蓝色,与酸变红色;酚酞遇碱性溶液变红色,与酸不变色进行分析;
根据碱与酸性氧化物和酸反应都能生成盐和水进行分析;
分析中和反应要从反应物和生成物的种类来判断.
解答 解:(1)碱会使紫色石蕊变蓝色,氢氧化钠和氢氧化钙溶液中具有相同的氢氧根离子,都能使紫色石蕊试液变蓝色,所以
| 氢氧化钠溶液 | 氢氧化钙溶液 | |
| 加紫色石蕊溶液 | 溶液变蓝 | 溶液变蓝 |
点评 本题重要考查了酸碱指示剂的变色反应及碱的化学性质和化学方程式的正确书写.


科目:初中化学 来源: 题型:解答题
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题

查看答案和解析>>
科目:初中化学 来源: 题型:填空题
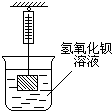 如图所示,弹簧称下悬挂一重物(不与氢氧化钡溶液和稀硫酸反应),若向氢氧化钡溶液中逐滴滴加稀硫酸至恰好完全反应,发生反应的化学方程式为Ba(OH)2+CuSO4═Cu(OH)2↓+BaSO4↓,反应结束后弹簧称的示数将变大.(填变大,变小,或不变)
如图所示,弹簧称下悬挂一重物(不与氢氧化钡溶液和稀硫酸反应),若向氢氧化钡溶液中逐滴滴加稀硫酸至恰好完全反应,发生反应的化学方程式为Ba(OH)2+CuSO4═Cu(OH)2↓+BaSO4↓,反应结束后弹簧称的示数将变大.(填变大,变小,或不变)查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.
在学校的元旦联欢会上,某同学表演了“水能生火”的魔术.他向包有过氧化钠(Na202)粉末的脱脂棉上滴水,脱脂棉燃烧起来.小蔡很感兴趣,于是,他和同学们进行探究.查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量样品于试管中,加入适量盐酸,塞上带导管的单孔塞,把导管插入盛有石灰水的试管中; | 有气体产生,气体使石灰水变浑浊 | 猜想2成立 |
| ②在上述反应后的试管中加少量品红溶液 | 品红溶液褪色 |
查看答案和解析>>
科目:初中化学 来源: 题型:选择题
| A. | Cr2(SO4)3 | B. | Cr2O3 | C. | K2Cr2O7 | D. | Cr(OH)3 |
查看答案和解析>>
科目:初中化学 来源: 题型:实验探究题
 图为氯化钠、硫酸镁和硝酸钾的溶解度曲线.
图为氯化钠、硫酸镁和硝酸钾的溶解度曲线.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com