
【题目】煤是重要的能源,也是生产化工产品的重要原料。随着人类社会的飞速发展,化石能源大量消耗,人类已经面临较严重的能源危机。为此,提高能源的利用率和开发更多的新能源显得相当重要。下图是煤化工产业链的一部分。
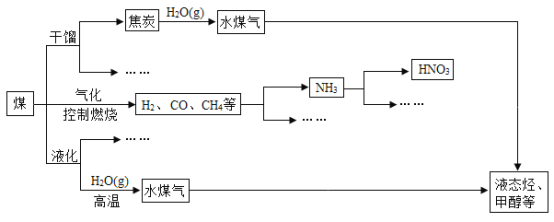
请回答:
(1)任意列举两种新能源______;
(2)上述处理煤的过程属于______(选填“物理”或“化学”)变化。
(3)煤和石油等化石燃料燃烧排放的大量二氧化碳会引起全球气候变暖。一种新的处理方法是将二氧化碳气体通人含有长石(地壳中最常见的矿石,含量高达60)成分的水溶液里,其中一种反应的化学方程式是:KAlSi3O8+CO2+2H2O=KHCO3+X↓+3SiO2↓,则X的名称是______;
(4)在煤燃烧前需对煤进行脱硫处理。煤的某种脱硫技术的原理如下图所示:
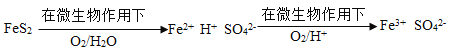
这种脱硫技术称为微生物脱硫技术。该技术的两步反应的化学方程式依次是:______。
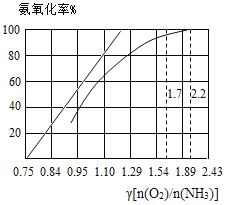
(5)工业上主要采用氨氧化法生产硝酸,如图是氨氧化率与氨—空气混合气中氧氨比的关系。其中直线表示反应的理论值;曲线表示生产实际情况。当氨氧化率达到100%,理论上γ[n(O2)/n(NH3)]=1.25,实际生产要将γ值维护在1.7 ~2.2之间,原因是________。
[温馨提示:n(O2)可以认为是表示氧气分子堆积数目的一种物理量,即n(O2)值越大,说明氧分子数目越多]
【答案】太阳能、氢能 化学 氢氧化铝 2FeS2+7O2+2H2O 2H2SO4+2FeSO4;2H2SO4+O2+4FeSO4
2H2SO4+2FeSO4;2H2SO4+O2+4FeSO4 2Fe2(SO4)3+2H2O 一方面提高氧气量,增大氨的氧化率;另一方面 γ 值在该范围,氨的氧化率已高达 95~99%, 再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本,所以而实际生产要将 γ 值 维持在 1.7~2.2 之间
2Fe2(SO4)3+2H2O 一方面提高氧气量,增大氨的氧化率;另一方面 γ 值在该范围,氨的氧化率已高达 95~99%, 再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本,所以而实际生产要将 γ 值 维持在 1.7~2.2 之间
【解析】
(1)常见的新能源有太阳能、地热能、氢能、风能、生物质能、核能等;
(2)煤的干馏、气化和液化都有新的物质产生,属于化学变化;
(3)根据化学方程式和质量守恒定律分析,反应前K:1个,反应后:1个,则x中不含K;反应前Al:1个,反应后应:1个,则x中含有一个Al,依此类推,x中还含有3个O,3个H,则X的化学式为 Al(OH)3,名称是氢氧化铝;
(4)第一步反应中反应物有FeS2、O2和H2O,生成物有Fe2+和SO42-,反应的方程式为:2FeS2+7O2+2H2O 2H2SO4+2FeSO4;Fe2+具有还原性,可被氧气氧化为Fe3+,方程式为:2H2SO4+O2+4FeSO4
2H2SO4+2FeSO4;Fe2+具有还原性,可被氧气氧化为Fe3+,方程式为:2H2SO4+O2+4FeSO4 2Fe2(SO4)3+2H2O;
2Fe2(SO4)3+2H2O;
(5)由氨氧化的化学方程式:4NH3+5O2 4NO+6H2O,可知氨氧化率达到100%,实际生产要将γ值维护在1.7-2.2之间,原因是浓度太少不利于NH3的转化,而γ值为2.2时NH3氧化率已近100%,再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本。
4NO+6H2O,可知氨氧化率达到100%,实际生产要将γ值维护在1.7-2.2之间,原因是浓度太少不利于NH3的转化,而γ值为2.2时NH3氧化率已近100%,再提高,氨的氧化率上升空间已有限,反而会增加能耗,提高生产成本。


科目:初中化学 来源: 题型:
【题目】实验设计能实现其对应的实验目的是
|
|
|
|
A. 测定空气中O2 的含量 | B. 证明 CO2 与NaOH溶液反应 | C. 比较 MnO2 和Fe2O3 的催化效果 | D. 此装置具有“启普发生器”的功能 |
A.AB.BC.CD.D
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图是初中化学中常见的实验。
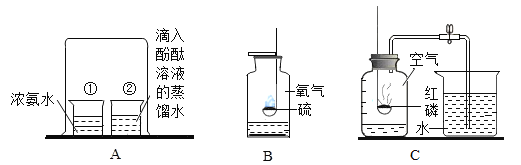
(1)A中现象:烧杯②中溶液变红。请用分子的知识解释“变红”的原因_____。
(2)B中集气瓶底部有少量水,其作用是_____。
(3)C实验完毕,集气瓶内水面上升到一定高度后,不能继续上升,这种现象说明氮气具有_____的性质;若从烧杯中进入集气瓶内水的体积明显小于瓶内原空气体积的![]() ,可能存在的原因是_____(写出一条即可)。
,可能存在的原因是_____(写出一条即可)。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】将 80g 某物质加入 50g 水中,充分溶解,测得溶液的质量随温度的变化曲线如图所示。
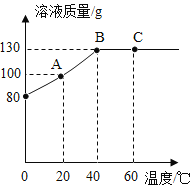
(1)20℃时,溶质质量分数为_____。
(2)40℃时,该物质的溶解度为_____。
(3)使 60℃时的饱和溶液析出晶体的方法为_____。(答出 1点即可)
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】如图实验装置进行的相应实验,不能达到实验目的的是( )
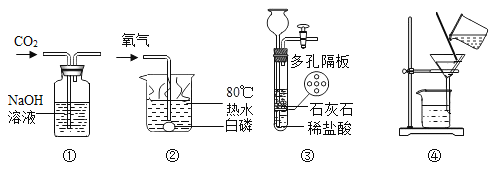
A.用①所示装置除去CO2中含有的少量HCl气体
B.用②所示装置证明可燃物燃烧需要与氧气接触
C.用③所示装置制取少量CO2气体
D.在实验室中,用④所示装置除去少量“七中墨池”水中的泥沙
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】人类每时每刻都离不开空气,没有空气就没有生命,就没有生机勃
(1)空气主要由氮气和氧气组成,还含有0.94%的_____等其他气体和杂质。
(2)为了保护空气,在我国新颁布的《环境空气质量标准》中,基本监控项目增设了PM2.5浓度限值,与该项目监测项目有关的是_____
A 二氧化硫 B 二氧化氮 C 一氧化碳 D 可吸入颗粒物
(3)如图所示装置用于测定空气中氧气的含量
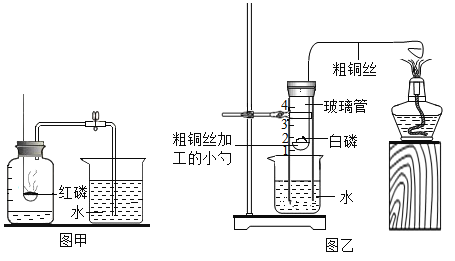
① 请补全下列实验步骤。
a.按图示连接好装置
b._____
c.在集气瓶内加入少量水,并将水面上方分为五等分,用弹簧夹夹紧胶皮管;
d.取足量红磷放入燃烧匙中,点燃后立即伸入瓶中,并把塞子塞紧;。
e.待红磷熄灭并冷却至室温后,打开弹簧夹。
② 红磷燃烧的现象是_____,反应的文字表达式为_____。
③ 若某同学在实验后得出结论:空气中氧气的体积约占1/5。能得出此结论的实验现象是_____。
④ 但实验结果液面往往偏低,其原因可能是_____(写一点)。
(4)图乙装置的优点_____。
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】能源和环境已经成为人民日益关注的问题.
(1)化石燃料主要包括煤、________和天然气.其中天然气的主要成分是________(填化学式).
(2)燃煤发电时,将煤块粉碎成煤粉,其目的是______.
(3)氢气作为理想的能源,其重要原因是它的燃烧产物无污染,用化学方程式 表示为_____.
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】在20℃时,刘冰同学向100g水中依次加入NaCl固体,充分溶解,实验过程如图所示。下列说法错误的是( )
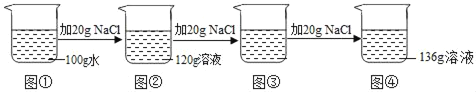
A. 图②中的溶液是不饱和溶液
B. 图③中的溶液是饱和溶液
C. 图③中溶液的溶质质量为40 g
D. 图③和图④中NaCl溶液的溶质质量分数相等
查看答案和解析>>
科目:初中化学 来源: 题型:
【题目】下图是部分固体物质溶解度曲线。据图回答下列问题。
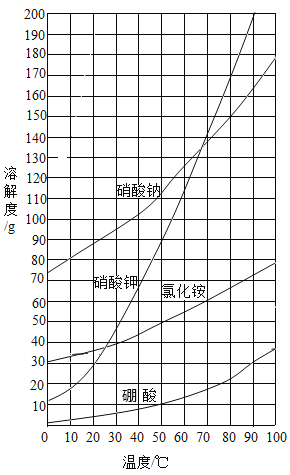
(1)查表,60°C时硝酸钾的溶解度约为_____g;
(2)40°C时,硝酸钠的溶解度比硼酸的_____(填 “大”或“小”);
(3)在保持温度不变的条件下,将一定量的氯化铵不饱和溶液均分成两等份,向其中一份中加入2.5g氯化铵,另一份蒸发5g水,均得到恰好饱和的溶液,则该温度氯化铵溶解度是_____g。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com